Continue sua leitura
Atezolizumabe aprovado para o tratamento do câncer de mama triplo- negativo no Brasil
Após a aprovação do uso de atezolizumabe para o tratamento do câncer de mama triplo-negativo no cenário americano, agora essa nova opção de tratamento chega a território nacional. A ANVISA (Agência Nacional de Vigilância Sanitária) aprovou em 13 de maio a indicação do anticorpo monoclonal anti-PDL-1 para o tratamento do câncer de mama subtipo triplo-negativo metastático em combinação com quimioterapia para pacientes cujo tumor apresente expressão positiva de PDL-1, conforme os dados do estudo IMpassion130.
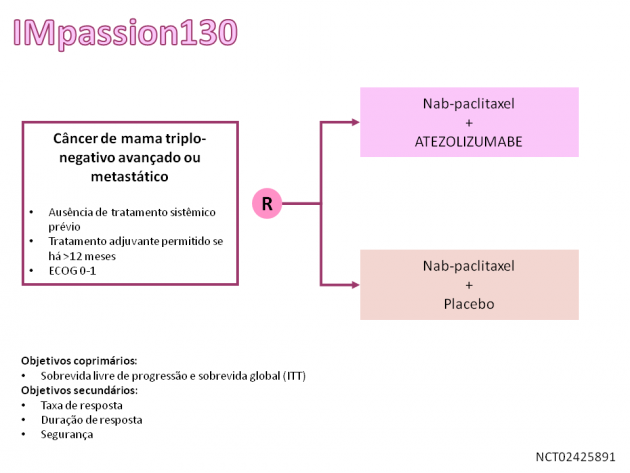
No estudo IMpassion130, 902 pacientes foram randomizadas para receber tratamento de primeira linha com nab-paclitaxel associado a atezolizumabe ou placebo, sendo permitida a inclusão de pacientes que haviam recebido taxano no cenário de doença localizada, desde que há mais de 12 meses. Na análise dos resultados da população por intenção de tratamento, com um seguimento mediano de 12,9 meses, o tratamento com nab-paclitaxel + atezolizumabe foi associado a uma redução relativa de 20% no risco de progressão ou morte quando comparado ao grupo de pacientes que receberam o quimioterápico associado a placebo (HR=0,80; IC de 95%: 0,69-0,92; p=0,002), objetivo primário do estudo. Dentre as pacientes com PDL-1 positivo (expressão ≥1% nas células imunes pelo anticorpo SP142 da Ventana), que correspondiam a cerca de 40% da população do estudo, o benefício em sobrevida livre de progressão foi ainda maior (HR=0,62; IC de 95%: 0,49-0,78; p<0,001).
A análise de sobrevida global, objetivo secundário do estudo, ainda é imatura, sendo os resultados expostos por ora exploratórios, com apenas 40% dos eventos reportados. Há, entretanto, sugestão de benefício para o tratamento combinado de nab-paclitaxel + atezolizumabe na população PDL-1 positiva, com sobrevida global mediana de 25 versus 15,5 meses (HR=0,62; IC de 95%: 0,45-0,86).
A taxa de resposta nas pacientes PDL-1 positivo foi da ordem de 58,9%, com 10,3% de respostas completas com o tratamento combinado, versus 42,6% e 1,1%, respectivamente, naquelas que receberam placebo. Nas análises de segurança, a taxa de eventos adversos de graus igual ou superior a 3 nas pacientes que receberam o imunoterápico foi de 48,7% versus 42,2% no grupo controle, destacando-se como os mais comuns neutropenia, neuropatia periférica, fadiga e anemia.
Conforme Dra. Juliana Martins Pimenta, oncologista da BP – A Beneficência Portuguesa de São Paulo, destaca: “trata-se de uma importante conquista para um subtipo de câncer de mama agressivo e de opções de tratamento mais limitadas. Um menor tempo para aprovação de importantes medicações pela ANVISA tem permitido que muitos pacientes se beneficiem mais rapidamente de novos tratamentos eficazes, e a possibilidade de selecionar um grupo de pacientes com maior chance de benefício permite otimizar recursos. A imunoterapia chega como opção de tratamento em primeira linha para o câncer de mama triplo-negativo metastático, com um pequeno grupo de pacientes com potencial resposta de longo prazo, como é visto com uso de imunoterapia em outros tipos de tumores e também com o tratamento anti-HER-2 em câncer de mama HER-2 positivo”.
Por Dr. Daniel Vargas P. de Almeida
Veja também:
- [Notícia] Imunoterapia aprovada para o tratamento do câncer de mama metastático nos EUA
- [Notícia] MOC 2019 | O que mudou nos capítulos de Mama
- [Vídeo] San Antonio 2018: Dr. Buzaid e Dras. Juliana Pimenta e Debora Gagliato – HIGHLIGHTS
- [Vídeo] San Antonio 2018: Dr. Buzaid e Dras. Juliana Pimenta e Debora Gagliato – Doença metastática
- [Vídeo] San Antonio 2018: Dra. Daniela Rosa – Diagnóstico e tratamento dos tumores HER-2 positivos
- [Vídeo] ESMO 2018: Dr. Carlos Barrios – Resultados do estudo IMpassion-130
- [Vídeo] ESMO 2018: Dra. Debora Gagliato – Resultados do estudo IMpassion-130
- [Vídeo] ESMO 2018: Dr. Carlos Barrios e Dra. Debora Gagliato – Estudos IMpassion-130 e SOLAR-1
- [Notícia] O que muda no MOC após a ESMO 2018
- [Notícia] Imunoterapia atinge resultado positivo em câncer de mama triplo-negativo
