Continue sua leitura
Tratamento adjuvante do câncer de mama com abemaciclibe é aprovado nos EUA
Em 12 de outubro de 2021, o FDA (Food and Drug Administration) aprovou o uso de abemaciclibe para o tratamento adjuvante do câncer de mama localizado com receptores hormonais positivos (RH positivo) e HER-2 negativo de risco alto com Ki-67 ≥ 20% à imunohistoquímica após cirurgia com intuito curativo.
A eficácia e a segurança do tratamento foram avaliadas no estudo de fase III monarchE, que randomizou 5.637 pacientes entre hormonioterapia padrão ou associada a abemaciclibe por 2 anos no tratamento adjuvante do câncer de mama RH positivo e HER-2 negativo de risco alto, após tratamento cirúrgico e/ou quimioterapia (neo ou adjuvante). O uso de quimioterapia ocorreu conforme indicação clínica. Dentre os critérios de inclusão do estudo, foram considerados tumores de risco alto aqueles com 1 a 3 linfonodos comprometidos apresentando tamanho ≥ 5 cm ou grau histológico 3 ou Ki-67 ≥ 20%, bem como aqueles com ≥ 4 linfonodos comprometidos, independente de outras características patológicas. O objetivo primário do estudo foi a sobrevida livre de doença invasiva (SLDI), desfecho que incorpora câncer de mama invasivo ipsilateral, recidiva de câncer de mama invasivo local ou regional, câncer de mama invasivo contralateral, segundo tumor primário invasivo não-câncer de mama, recidiva à distância ou morte por qualquer causa.
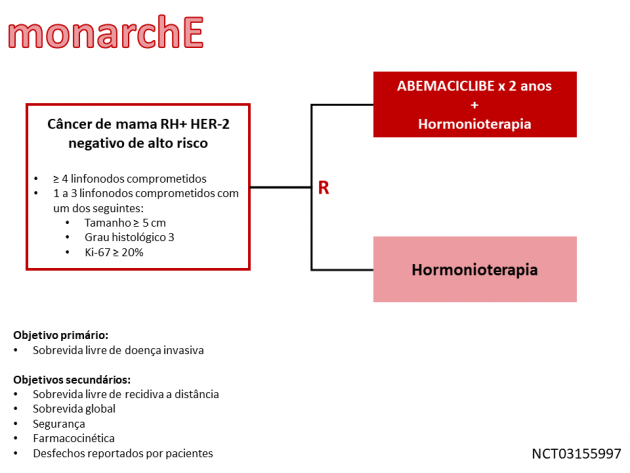
Na análise da população com Ki-67 ≥ 20% (n=2003), a adição de abemaciclibe por 2 anos ao tratamento hormonal adjuvante foi associada a benefício estatisticamente significativo na sobrevida livre de doença invasiva (HR=0,626; IC de 95%: 0,488-0,803; p=0,042), com taxas de 86,1% versus 79,0% aos 3 anos nos braços abemaciclibe e terapia hormonal isolada, respectivamente. Os dados de sobrevida global ainda são imaturos. Os eventos adversos que ocorreram em maior frequência no braço abemaciclibe foram diarreia, infecções, neutropenia, fadiga, leucopenia, náuseas, anemia e cefaleia.
Sobre a aprovação, Dra. Debora Gagliato, oncologista clínica da BP – A Beneficência Portuguesa de São Paulo, comenta: “trata-se de um ganho importante para pacientes com expressão de receptor hormonal e de risco alto de recidiva, em que, apesar do uso de quimioterapia citotóxica e terapia endócrina, ainda podem apresentar um risco alto de recorrência da doença. Ressaltamos que a taxa de recorrência invasiva no braço terapia endócrina isolada (aproximadamente 95% delas receberam quimioterapia), foi de 16,6% após 3 anos, demonstrando que o estudo recrutou de fato uma população de risco altíssimo. No estudo monarchE, abemaciclibe foi capaz de reduzir o risco de recidiva precoce, sugerindo impacto em pacientes com poderiam desenvolver resistência hormonal primária. Com o atual acompanhamento mediano de 27 meses, abemaciclibe combinado à terapia endócrina continua a oferecer um benefício clinicamente significativo em recidiva invasiva e à distância, que se estendeu além do período de tratamento de 2 anos. Há, no entanto, grande importância e interesse em um seguimento mais prolongado e na avaliação de sobrevida global neste estudo”.
Por Dr. Daniel Vargas P. de Almeida
Veja também:
- [NOTÍCIA] Abemaciclibe é aprovado para o tratamento adjuvante do câncer de mama inicial no Brasil
- [VÍDEO] Incorporação de abemaciclibe ao Rol da ANS – Um ganho para as pacientes com câncer de mama avançado
- [NOTÍCIA] Abemaciclibe é incorporado ao Rol da ANS
- [VÍDEO-MOC] VOLUME 12 ● NÚMERO 10 – Abemaciclibe em câncer de mama localizado RH positivo HER-2 negativo (Estudo MONARCHE)
- [PODCAST] Podcast #049 – Novo Rol ANS | Comentários sobre as atualizações no cenário da oncologia
