Continue sua leitura
Trastuzumabe deruxtecana recebe aprovação para o tratamento do câncer de mama HER-2 low nos EUA
O FDA (Food and Drug Administration) aprovou em 05 de agosto de 2022 o uso do anticorpo conjugado a droga (ACD) trastuzumabe deruxtecana (T-DXd) para o tratamento de pacientes com câncer de mama metastático HER-2 low após exposição a pelo menos um regime quimioterápico para a doença avançada ou no caso de doença recidivada em até 6 meses após o término do tratamento quimioterápico adjuvante.
Esta aprovação foi baseada nos dados do estudo DESTINY-Breast04 que randomizou 557 pacientes com câncer de mama HER-2 low metastático ou irressecável entre tratamento com T-DXd ou quimioterapia a escolha do investigador (eribulina, capecitabina, gencitabina, nab-paclitaxel ou paclitaxel). A doença classificada como HER-2 low corresponde àquela com resultado da análise imuno-histoquímica para HER-2 1+ ou 2+ com teste de hibridização in situ negativo. Cerca de 90% dos pacientes possuíam doença com expressão de receptores hormonais (RH+), dois terços apresentavam metástases hepáticas, 5% com metástases cerebrais e 60% deles haviam recebido ao menos três linhas de tratamento prévias para a doença metastática.
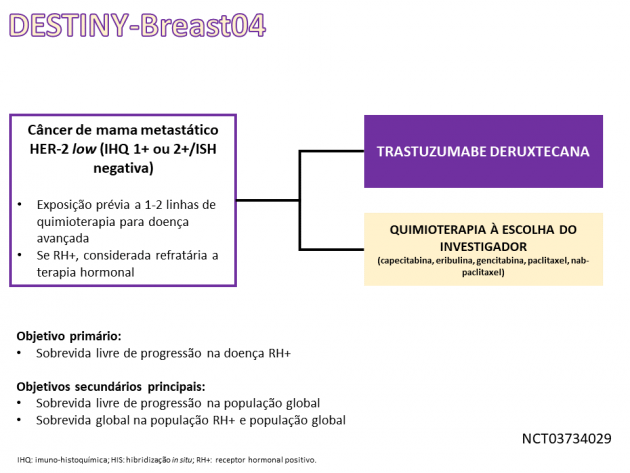
O estudo atingiu seu objetivo primário, demonstrando redução de 49% no risco de progressão ou morte em favor de T-DXd nos pacientes com doença RH+ (HR=0,51; IC de 95%: 0,40-0,64; p<0,001). Quando a análise foi conduzida na população global, o resultado também foi favorável ao braço do ACD (HR=0,50; IC de 95%: 0,40-0,63; p<0,001). Adicionalmente, o braço randomizado para tratamento com T-DXd também demonstrou resultados positivos na avaliação de sobrevida global na população RH+ (HR=0,64; IC de 95%: 0,48-0,86; p=0,003) e na população global (HR=0,64; IC de 95%: 0,49=0,84; p=0,001). Na avaliação dos pacientes com RH-, a performance do braço experimental também foi superior ao braço controle na sobrevida livre de progressão (HR=0,46; IC de 95%: 0,24-0,89) e na sobrevida global (HR=0,48; IC de 95%: 0,24-0,95). Na população global, a taxa de resposta a T-DXd foi 52,3% versus 16,3% nos pacientes que receberam quimioterapia. Na avaliação de segurança, a taxa de eventos adversos de graus ≥ 3 foi 52,6% versus 67,4% para o ACD e quimioterapia, respectivamente, com destaque para toxicidades mais frequentes no braço experimental náuseas, fadiga e alopecia. A taxa de doença intersticial pulmonar com o ACD foi 12,1%, com 2,1% de eventos de graus ≥ 3. Em relação à segurança cardiológica, 11,9% dos pacientes tratados com T-DXd apresentaram queda da fração de ejeção do ventrículo esquerdo de grau 2 (redução de 10-19% do basal) e 1,5% de grau 3 (redução > 20% do basal).
A Dra. Debora Gagliato, oncologia da BP – A Beneficência Portuguesa de São Paulo, comenta: “O estudo DESTINY-Breast04 reformula a forma como o câncer de mama é classificado e tratado. Previamente a esse estudo, uma terapia dirigida contra HER-2 nunca havia demonstrado benefício em pacientes com câncer de mama metastático com baixa expressão de HER-2. Nesse grupo de pacientes, trastuzumabe deruxtecana foi associado à duplicação da sobrevida livre de progressão, juntamente com um ganho de 6 meses na sobrevida global, em comparação à quimioterapia, o que claramente altera a prática clínica de tratamento vigente. O tratamento é ativo independentemente do status de receptor hormonal, sítios de metástases, linhas de tratamento prévias, e expressão de HER-2 1+ ou 2+”.
Por Dr. Daniel Vargas P. de Almeida
Veja também:
- [NOTÍCIA] Nova indicação de uso de trastuzumabe deruxtecana aprovada pela ANVISA
- [NOTÍCIA] Trastuzumabe deruxtecana recebe designações positivas do FDA
- [NOTÍCIA] Trastuzumabe deruxtecana recebe aprovação definitiva nos EUA
- NOTÍCIA] Trastuzumabe deruxtecana recebe revisão prioritária para o tratamento de segunda linha do câncer de mama HER-2 positivo avançado pelo FDA
- [NOTÍCIA] Trastuzumabe deruxtecana é aprovado pela ANVISA para o tratamento do câncer de mama HER-2 positivo avançado
- [VÍDEO-MOC] VOLUME 12 ● NÚMERO 12 – TRASTUZUMABE DERUXTECANA EM CÂNCER DE MAMA (ESTUDO DESTINY-BREAST01)
