Continue sua leitura
Pembrolizumabe é aprovado como nova opção de tratamento adjuvante do melanoma
Em fevereiro de 2019, o anticorpo monoclonal anti-PD-1 pembrolizumabe recebeu a aprovação da ANVISA (Agência Nacional de Vigilância Sanitária) para o tratamento adjuvante após ressecção cirúrgica do melanoma, tumor que figura como o 5º de maior incidência nas estatísticas americanas e representa cerca 5% dentre todos os tipos de câncer naquele país.
A aprovação é baseada nos dados do estudo randomizado de fase III KEYNOTE-054, que avaliou o uso de pembrolizumabe ou placebo, ambos por 1 ano, em 1.019 pacientes com melanoma localmente avançado (estádio III) após serem submetidos à cirurgia com ressecção completa do tumor.
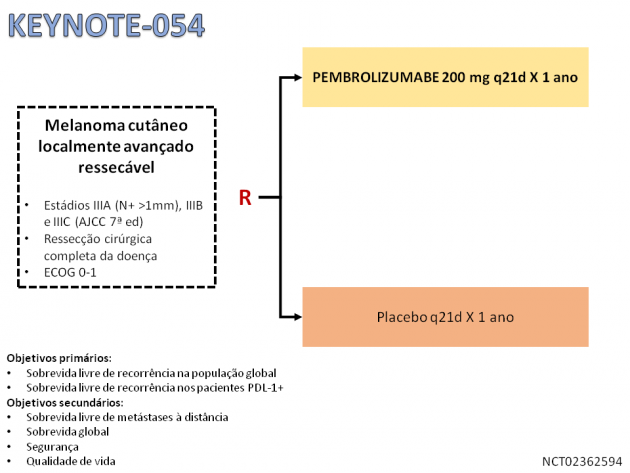
Com um seguimento mediano de 15 meses, o uso de pembrolizumabe foi associado a uma redução relativa de 43% no risco de recidiva ou morte quando comparado ao grupo de pacientes que recebeu placebo (HR=0,57; IC de 98,4%: 0,43-0,74; p<0,001). As curvas de sobrevida livre de recorrência, objetivo principal do estudo, demonstram uma tendência a atingir um platô, com 75,4% dos pacientes vivos e sem recorrência aos 12 meses, e taxa de 71,4% aos 18 meses de seguimento. A análise da sobrevida livre de recorrência nos pacientes com expressão de PDL-1 >1%, um objetivo coprimário do estudo, também demonstrou resultado semelhante (HR=0,54; IC de 95%: 0,42-0,69; p<0,001).
No que diz respeito à segurança, a taxa de efeitos adversos com o uso de pembrolizumabe foi semelhante aos dados da utilização da droga em outros cenários da doença, com eventos relacionados à droga de graus ≥3 em 14,7% dos pacientes, sendo os principais fadiga, reações cutâneas, colite e artralgia.
“A aprovação do pembrolizumabe para pacientes com estádio III é de grande importância, visto que pembrolizumabe demonstrou uma redução no risco recidiva ou morte muito maior que interferon (43% versus ~15%), além de menos efeitos colaterais. Inequivocamente um grande avanço”, afirma Dr. Antonio Carlos Buzaid, Diretor Médico Geral do Centro de Oncologia da BP – A Beneficência Portuguesa de São Paulo e Membro do Comitê Gestor do Centro de Oncologia do Hospital Israelita Albert Einstein.
Por Dr. Daniel Vargas P. de Almeida
Veja também:
