Continue sua leitura
Nova droga é aprovada para o tratamento do câncer de pulmão com mutação de EGFR éxon 20 nos EUA
No dia 15 de setembro de 2021, o FDA (Food and Drug Administration) concedeu aprovação acelerada ao inibidor de EGFR mobocertinibe para o tratamento de pacientes portadores de câncer de pulmão localmente avançado ou metastático com mutação de EGFR no éxon 20 após progressão a um regime quimioterápico baseado em platina.
Os dados utilizados para a aprovação são derivados do Estudo 101, que avaliou o tratamento com mobocertinibe em 114 pacientes com câncer de pulmão de células não pequenas apresentando mutação do EGFR no éxon 20 após tratamento com quimioterapia baseada em platina. Dentre a população avaliada, 35% dos pacientes possuíam metástase cerebral e 43% deles havia recebido imunoterapia previamente.
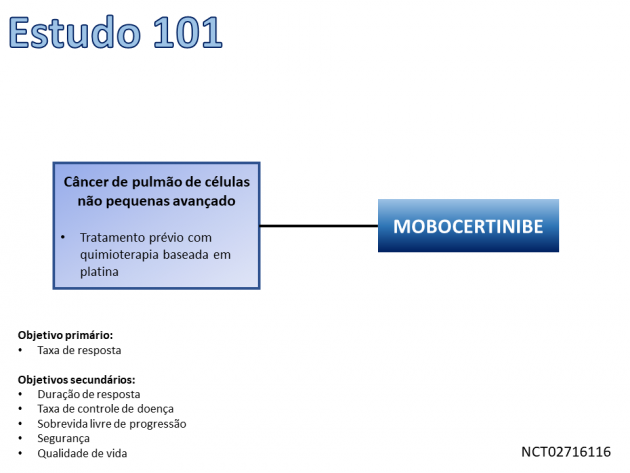
A taxa de resposta ao inibidor de tirosina quinase foi 28%, com duração mediana de resposta de 17,5 meses. As toxicidades mais frequentes à droga foram diarreia, rash, náusea, estomatite, vômito, redução do apetite, paroníquia, fadiga, xerodermia e dor musculoesquelética. Na bula do medicamento, também há destaque para o risco de toxicidades graves menos frequentes como prolongamento do intervalo QTc, Torsades de Pointes, doença pulmonar intersticial/pneumonite, toxicidade cardiológica e diarreia.
“O mobocertinibe é o primeiro inibidor de tirosina quinase oral projetado para atuar seletivamente nas mutações do EGFR do tipo inserção no éxon 20. Sua aprovação nos permite oferecer a esta população de pacientes, que até então carecia de tratamentos eficazes, uma terapia direcionada com respostas clinicamente significativas e sustentadas“, destaca a Dra. Suellen Nastri Castro, oncologista da BP – A Beneficência Portuguesa de São Paulo.
Por Dr. Daniel Vargas P. de Almeida
