Continue sua leitura
Nova indicação de tratamento com imunoterapia para o câncer de pulmão avançado no Brasil
O uso de inibidores de checkpoint para o tratamento do câncer de pulmão de células não pequenas avançado recebeu a aprovação de uma nova indicação pela ANVISA (Agência Nacional de Vigilância Sanitária) em 09 de setembro de 2019. Previamente, o tratamento com pembrolizumabe na primeira linha era aprovado apenas quando associado a quimioterapia, conforme os resultados do estudo KEYNOTE-189, ou como monoterapia apenas em pacientes com expressão de PDL-1 ≥ 50% baseado no estudo KEYNOTE-024. A nova indicação de uso é baseada no estudo fase III KEYNOTE-042, e expande o uso de pembrolizumabe em monoterapia para pacientes com doença localmente avançada ou metastática e PDL-1 ≥ 1%.
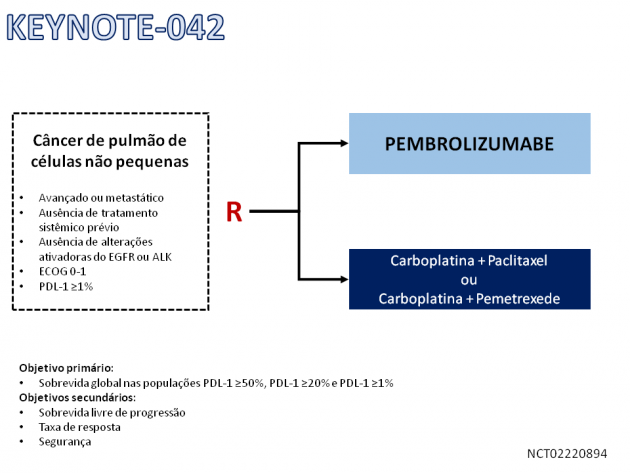
Os resultados do estudo clínico que motivaram essa nova aprovação foram demonstrados através do tratamento de 1.274 pacientes com câncer de pulmão de células não pequenas avançado com expressão de PDL-1 (TPS – tumor proportion score) ≥ 1% que foram randomizados para receber tratamento de primeira linha com pembrolizumabe em monoterapia ou quimioterapia baseada em dupla de platina. Destaca-se que nesse estudo não foi permitida a inclusão de pacientes com alterações ativadoras do EGFR ou ALK. A análise final dos resultados apresentada no Congresso Europeu de Câncer de Pulmão de 2019, após um seguimento mediano de 14 meses demonstrou que o tratamento com pembrolizumabe reduziu o risco relativo de morte em 18% quando comparado ao tratamento quimioterápico na população total incluída no estudo (HR=0,82; IC de 95%: 0,71-0,93). Quando analisados os pacientes com PDL-1 ≥ 20% e PDL-1 ≥ 50%, o tratamento foi associado a um benefício em sobrevida global diretamente proporcional à expressão do marcador (HR=0,77 e HR=0,70, respectivamente). Uma análise exploratória conduzida nos pacientes com expressão de PDL-1 entre 1-49% demonstra que embora pembrolizumabe não tenha sido superior a quimioterapia convencional nesta população (HR=0,91; IC de 95%: 0,77-1,09), a imunoterapia pode ter um papel importante naqueles pacientes em que a quimioterapia não é desejável.
A taxa de resposta na população com PDL-1 ≥ 1% foi de 27% em ambos os braços de tratamento, entretanto a duração mediana de resposta naqueles que receberam pembrolizumabe foi de 20,2 meses, já naqueles tratados com quimioterapia a duração mediana do benefício foi de 8,4 meses.
Nas análises de segurança, a taxa de eventos adversos de graus igual ou maior a 3 relacionados ao tratamento foi de 18% com pembrolizumabe versus 41% com quimioterapia, destacando-se como eventos adversos mais comuns fadiga, dispneia, tosse, alterações do hábito intestinal e disfunções da tireoide.
“O estudo KEYNOTE-042 demonstra que o pembrolizumabe é uma sólida opção de tratamento de primeira linha para pacientes com câncer de pulmão de células não pequenas avançado, histologia escamosa e não escamosa, EGFR e ALK negativos e PDL-1 positivo. Além de consolidar os dados do KEYNOTE-024, tal estudo permite o uso do pembrolizumabe como monoterapia também nos tumores com expressão de PDL-1 entre 1 e 49%, especialmente na população de pacientes em que a combinação de pembrolizumabe com quimioterapia não é factível”, comenta a Dra. Carolina Kawamura Haddad, oncologista da BP, A Beneficência Portuguesa de São Paulo.
Por Dr. Daniel Vargas P. de Almeida
