Continue sua leitura
Tratamento neoadjuvante do câncer de pulmão com imunoterapia é aprovado nos EUA
O FDA (Food and Drug Administration) aprovou em 04 de março de 2022 o uso de nivolumabe em combinação a quimioterapia com dupla de platina para o tratamento neoadjuvante de pacientes com câncer de pulmão de células não pequenas localizado apresentando doença ressecável. Trata-se da primeira aprovação pela agência de uma terapia neoadjuvante para a doença inicial localizada.
A aprovação foi embasada nos dados do estudo de fase III CheckMate-816, que avaliou o tratamento neoadjuvante em pacientes com diagnóstico de câncer de pulmão de células não pequenas estádios IB (≥ 4 cm) a IIIA sem alterações sensibilizadoras de ALK ou EGFR. Foram randomizados 358 pacientes a uma razão 1:1 entre três ciclos neoadjuvantes de quimioterapia baseada em dupla de platina associada ou não a nivolumabe na dose de 360 mg, via intravenosa, a cada 3 semanas. A cirurgia foi realizada dentro de 6 semanas após a conclusão do tratamento neoadjuvante e o uso de quimioterapia e radioterapia adjuvantes foi permitido a critério do investigador.
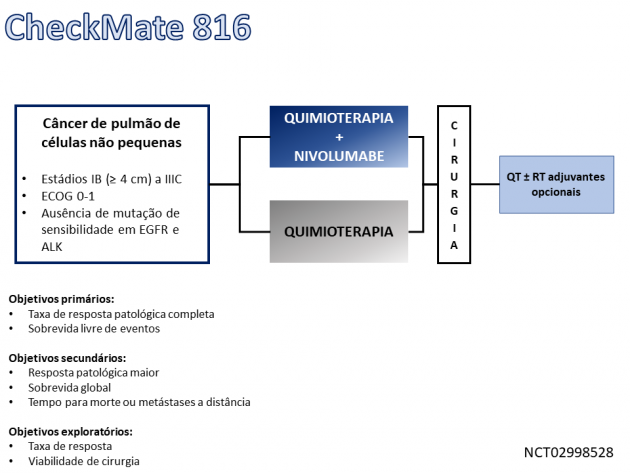
A taxa de resposta patológica completa, um dos objetivos primários do estudo, foi de 24% versus 2,2% nos braços com e sem nivolumabe, respectivamente. Quando analisados apenas os pacientes submetidos a cirurgia, a taxa de resposta patológica completa foi de 30,5% no braço que recebeu nivolumabe versus 3,2% dentre os que receberam apenas quimioterapia.
A sobrevida livre de eventos mediana foi de 31,6 versus 20,8 meses nos braços de quimioimunoterapia e quimioterapia, respectivamente, representando uma redução de 37% no risco de eventos (HR=0,63; IC de 95%: 0,43-0,91; p=0,0052). O braço que recebeu o tratamento combinado não teve acréscimo nas taxas de toxicidades de graus 1-2 ou ≥ 3, bem como não foi associado a maior frequência de cancelamentos ou atrasos no tratamento cirúrgico. Os eventos adversos mais incidentes dentre os pacientes que receberam nivolumabe foram náuseas, constipação, fadiga, redução do apetite e rash cutâneo.
Conforme destaca o Dr. William William, oncologista e diretor médico da Oncologia Clínica e Hematologia do Centro Oncológico da BP – A Beneficência Portuguesa de São Paulo, “o estudo CheckMate-816 representa mais um passo importante na incorporação de imunoterapia peri-operatória para câncer de pulmão de células não pequenas. Depois de décadas sem o desenvolvimento de novas estratégias para essa população de pacientes curáveis, a imunoterapia vai se tornando um novo padrão com o potencial de alterar os desfechos significativamente, especialmente para pacientes sem mutações em genes driver”.
Por Dr. Daniel Vargas P. de Almeida
