Continue sua leitura
Tratamento de sarcoma raro recebe nova aprovação nos EUA
Em 22 de novembro de 2021, o FDA (Food and Drug Administration) aprovou o agente sirolimus em formulação ligada a proteínas (nab-sirolimus) para o tratamento de pacientes com diagnóstico de tumor de células epitelióides perivasculares (PEComa) apresentando doença localmente avançada irressecável ou metastática.
A eficácia do tratamento com nab-sirolimus foi avaliada no estudo AMPECT, que incluiu 31 pacientes com diagnóstico de PEComa localmente avançado irressecável ou metastático. Dentre a população avaliada, os sítios primários de doença apresentados em maior frequência foram útero (24%), pelve (18%), retroperitônio (18%), pulmão (12%) e rim (12%); 85% dos pacientes apresentavam doença metastática e 12% deles haviam recebido tratamento sistêmico prévio para a doença avançada.
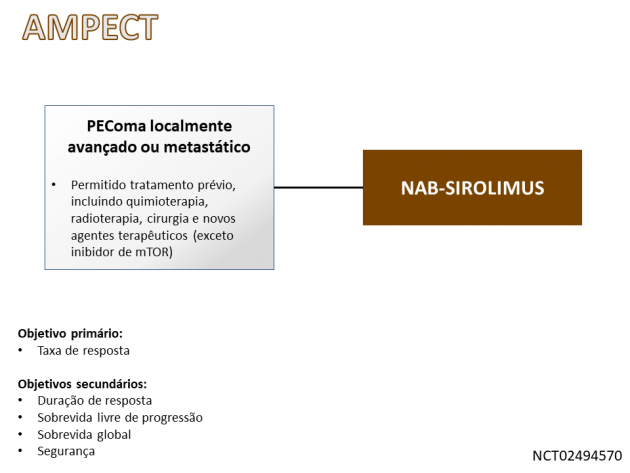
A taxa de resposta, objetivo primário do estudo, foi de 39%, incluindo respostas completas apresentadas por dois pacientes. A duração mediana de resposta não foi alcançada, porém 67% e 58% dos respondedores mantiveram o benefício por ao menos 12 e 24 meses, respectivamente. Na avaliação de segurança, os eventos adversos reportados em maior frequência foram estomatite, fadiga, rash cutâneo, infecção, náuseas, edema, diarreia, dor musculoesquelética, redução do apetite, tosse, êmese e disgeusia.
A dose de tratamento recomendada é nab-sirolimus 100 mg/m2, via intravenosa, nos dias 1 e 8 a cada 21 dias até progressão de doença ou toxicidade limitante.
Por Dr. Daniel Vargas P. de Almeida
