Continue sua leitura
Tratamento adjuvante do câncer de pulmão com atezolizumabe é aprovado no Brasil
A ANVISA (Agência Nacional de Vigilância Sanitária) aprovou em 25 de novembro de 2021 o uso do imunoterápico atezolizumabe para o tratamento adjuvante de pacientes com diagnóstico de câncer de pulmão de células não pequenas (CPCNP) estádios II a IIIA com expressão de PDL-1 ≥ 1% nas células tumorais após ressecção cirúrgica com intuito curativo e quimioterapia adjuvante baseada em platina.
Essa nova indicação de tratamento com atezolizumabe é baseada nos resultados do estudo IMpower010, que randomizou 1.005 pacientes com CPCNP estádios IB (T ≥ 4 cm) a IIIA submetidos a cirurgia e quimioterapia adjuvante com platina para receber atezolizumabe ou melhor cuidado de suporte. Os esquemas de quimioterapia adjuvante permitidos consistiam nas combinações de cisplatina com vinorelbina, docetaxel, gencitabina ou pemetrexede (este último, apenas para pacientes com doença de histologia não escamosa). O tratamento adjuvante com atezolizumabe foi administrado após o término da quimioterapia na dose de 1.200 mg, via intravenosa, a cada 3 semanas por 16 ciclos. A avaliação da expressão de PDL-1 foi realizada com o uso do anticorpo SP263. Dentre a população incluída, a maioria dos pacientes possuía histologia não escamosa (66%), cerca de três quartos dos pacientes (78%) apresentavam história de tabagismo atual ou prévio e aproximadamente 15% dos pacientes possuíam mutações de EGFR ou ALK.
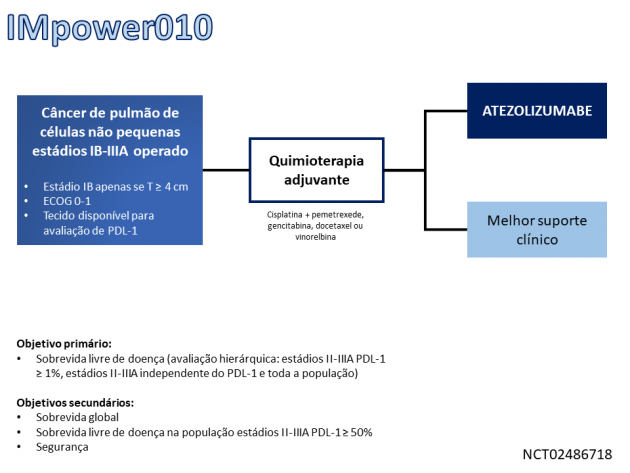
O tratamento adjuvante com atezolizumabe reduziu em 34% o risco de recidiva de doença ou morte na população com doença estádios II-IIIA com expressão de PDL-1 ≥ 1% (HR=0,66; IC de 95%: 0,50-0,88; p=0,004), objetivo primário do estudo. A avaliação de sobrevida livre de doença também foi conduzida em todos os pacientes com doença estádios II-IIIA (HR=0,79; IC de 95%: 0,64-0,96; p=0,02) e em toda a população por intenção de tratamento (HR=0,81; IC de 95%: 0,67-0,99; p=0,04), porém sem atingir o nível de significância estatística pré-determinada nesta última. A taxa de eventos adversos de graus ≥ 3 foi superior no braço de atezolizumabe (22% versus 12%), com 8% de toxicidades imuno-mediadas de graus ≥ 3.
“Esse é o primeiro estudo de fase III a demonstrar o beneficio da imunoterapia em pacientes com CPNPC estádios iniciais operados. Os dados acima demonstram claramente o benefício dessa estratégia após quimioterapia adjuvante em pacientes com estádios II e IIIA com alta expressão de PDL-1, além de haver um racional que nos traz expectativas de que o benefício seja prolongado, como é característico dos tratamentos utilizando esta classe de drogas. Com essa aprovação, atezolizumabe torna-se o padrão de tratamento para este cenário”, destaca a Dra. Suellen Nastri Castro, oncologista da BP – A Beneficência Portuguesa de São Paulo.
Por Dr. Daniel Vargas P. de Almeida
Veja também:
