Continue sua leitura
Terapia-alvo aprovada para o tratamento de tumor pediátrico raro nos EUA
A neurofibromatose tipo 1 é uma doença neurogenética de etiologia hereditária autossômica dominante. Dentre os comemorativos clínicos associados à doença, destacam-se lesões pigmentadas cutâneas e alterações neurológicas e musculoesqueléticas. Até metade dos pacientes portadores dessa doença desenvolvem neurofibromas plexiformes, um tumor que envolve a bainha dos nervos periféricos, usualmente associado à limitação funcional e dores decorrentes do crescimento local. O FDA (Food and Drug Administration) aprovou em 10 de abril o uso de selumetinibe, um inibidor de MEK de administração oral para o tratamento de pacientes pediátricos (a partir de 2 anos) com neurofibroma plexiforme não ressecável cirurgicamente.

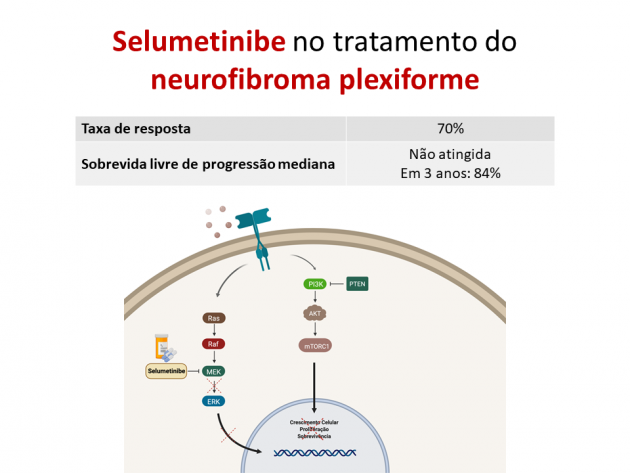
A aprovação é baseada nos resultados do estudo clínico de fase II SPRINT, que avaliou selumetinibe na dose de 25 mg/m2, por via oral, duas vezes ao dia até progressão de doença ou toxicidade limitante no tratamento de 50 pacientes pediátricos com neurofibroma plexiforme irressecável. O tratamento promoveu uma taxa de resposta confirmada de 70%, com duração do benefício por ao menos 12 meses em 80% dos respondedores. Adicionalmente, o uso de selumetinibe foi associado a benefício em escores de avaliação de dor, qualidade de vida e capacidade funcional (força e amplitude de movimento). Na análise de segurança, a maioria dos eventos adversos foi de graus 1 ou 2, destacando-se como mais frequentes: náuseas, vômito, diarreia, elevação assintomática de creatinofosfoquinase (CPK), rash acneiforme e paroníquia.
Por Dr. Daniel Vargas P. de Almeida
