Continue sua leitura
Quimioterapia associada a atezolizumabe e bevacizumabe é aprovada para o tratamento do câncer de pulmão avançado nos EUA
O tratamento do câncer de pulmão de células não pequenas avançado de histologia não escamosa recebeu a aprovação de uma nova opção de tratamento pela agência norte-americana Food and Drug Administration (FDA) no dia 06 de dezembro de 2018. O regime quimioterápico combinado de carboplatina e paclitaxel associado aos anticorpos monoclonais atezolizumabe e bevacizumabe foi aprovado para o tratamento de primeira linha dos pacientes com ausência de alterações no ALK ou EGFR, baseado nos dados do estudo de fase III IMpower-150.
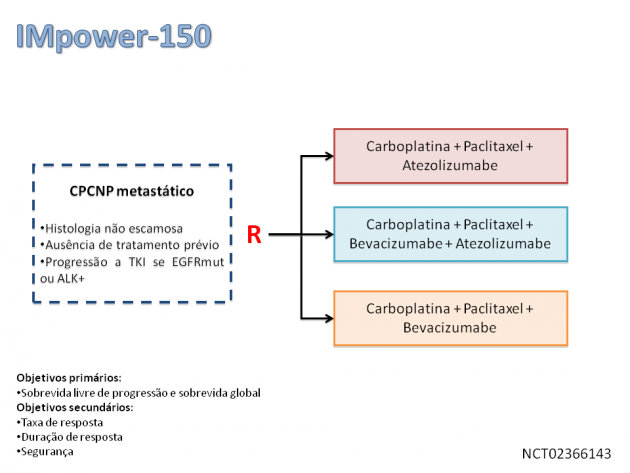
Nesse estudo, 1202 pacientes com câncer de pulmão de células não pequenas metastático de histologia não escamosa foram randomizados para receber um dentre três diferentes regimes de tratamento de primeira linha: carboplatina + paclitaxel + atezolizumabe + bevacizumabe (braço 1), carboplatina + paclitaxel + atezolizumabe (braço 2), ou carboplatina + paclitaxel + bevacizumabe (braço 3). Foi permitida a inclusão de pacientes com alterações no ALK ou EGFR caso apresentassem progressão ao tratamento prévio com inibidor de tirosina quinase. O tratamento quimioterápico foi administrado por 4-6 ciclos, sendo então modificado para a manutenção com atezolizumabe e/ou bevacizumabe de acordo com os regimes de tratamento inicialmente propostos. Com um seguimento mediano de cerca de 15 meses, os pacientes com ausência de mutações driver tratados com o regime de quatro drogas (braço 1) apresentaram benefício estatisticamente significante em sobrevida livre de progressão (HR=0,62; IC de 95%: 0,52-0,74; p<0,001), bem como em sobrevida global (HR=0,78; IC de 95%: 0,64-0,96; p=0,02) quando comparados aos que receberam regime padrão de três drogas (braço 3). A taxa de resposta atingida também foi numericamente superior para o braço 1 quando comparado ao braço 3 (55% versus 42%). No tocante a segurança, a taxa de eventos adversos sérios foi de 25,4% no braço 1 e 19,3% no braço 3. Os eventos adversos mais comuns foram fadiga, alopecia, náusea, diarreia, constipação, inapetência, artralgia, hipertensão e neuropatia. As demais toxicidades foram semelhantes ao dados prévios da utilização dessas drogas em outros cenários.
“Este é mais um passo importante no desenvolvimento de tratamentos baseados em imunoterapia para o câncer de pulmão de células não pequenas (CPCNP). As taxas de resposta da combinação de carboplatina, paclitaxel, bevacizumabe e atezolizumabe estão entre as mais altas já vistas em primeira linha para pacientes não mutados, e o aumento na sobrevida global justifica essa combinação como mais uma opção padrão para os pacientes com CPCNP não escamoso metastático virgens de tratamento” conforme ressalta o Dr. William William, oncologista e diretor médico da Oncologia Clínica e Hematologia do Centro Oncológico da BP – A Beneficência Portuguesa de São Paulo.
Ainda de acordo com a Dra. Carolina Kawamura Haddad, oncologista da BP – A Beneficência Portuguesa de São Paulo, “o estudo IMpower-150 incluiu pacientes com alterações de EGFR/ALK, contudo uma emenda posterior alterou o objetivo primário do estudo para a análise apenas dos pacientes com ausência de mutação driver. Entretanto, os desfechos nesses pacientes devem ser analisados no futuro breve, muito embora os dados atuais sugiram benefício também nesta população”.
Por Dr. Daniel Vargas P. de Almeida
