Continue sua leitura
Nova opção de tratamento adjuvante para o câncer de mama HER-2 positivo aprovado no Brasil
A câncer de mama é a neoplasia de maior prevalência na população feminina no Brasil (excluindo-se os tumores de pele não-melanoma), correspondendo a cerca de um terço dos novos tumores nessa população anualmente. As estatísticas brasileiras apontam para aproximadamente 59.700 novos casos no ano de 2018, com aproximadamente 15.000 mortes em decorrência da doença no território nacional durante o mesmo período. Dentre os subtipos de câncer de mama, aqueles com amplificação ou superexpressão de HER-2 correspondem a cerca de 15-20% e são os tumores cuja história natural vem sendo drasticamente modificada a partir do desenvolvimento das terapias alvo-dirigidas.
No dia 09 de julho de 2019, a ANVISA (Agência Nacional de Vigilância Sanitária) divulgou a aprovação de T-DM1 (trastuzumabe emtansina) para o tratamento adjuvante do câncer de mama inicial HER-2 positivo nas pacientes que apresentaram doença residual após tratamento com terapia anti-HER2 combinado à quimioterapia neoadjuvante, de acordo com os dados do estudo de fase III KATHERINE.
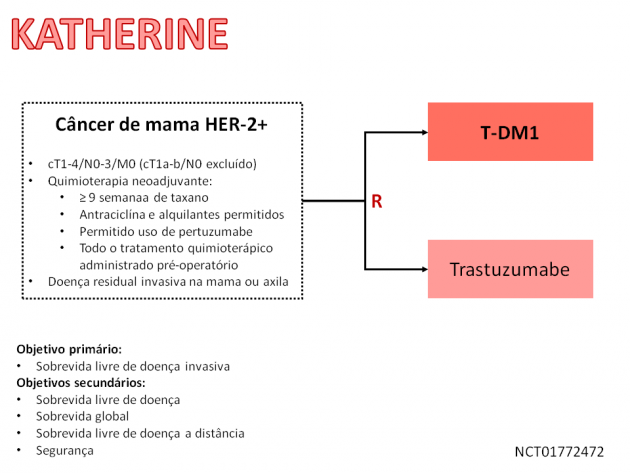
Nesse estudo, foi avaliado tratamento adjuvante de 1486 pacientes, as quais foram randomizadas 1:1 para receber T-DM1 ou trastuzumabe por 14 ciclos, após apresentarem falha na obtenção de resposta patológica completa (em mama ou linfonodos axilares) com tratamento quimioterápico neoadjuvante prévio (baseado em poliquimioterapia com taxano e trastuzumabe, com ou sem associação de pertuzumabe). Em análise interina dos dados, com seguimento mediano de 40 meses, o estudo atingiu seu desfecho primário, promovendo uma redução relativa de 50% no risco de recorrência de doença invasiva ou morte, no grupo tratado com T-DM1 em detrimento de trastuzumabe na adjuvância. Houve ainda 40% de redução no risco de recidiva à distância no grupo tratado com o anticorpo conjugado à droga. Os dados de sobrevida global ainda são imaturos na presente análise, mas já parecem indicar abertura das curvas de sobrevida, favorecendo uso de T-DM1. Nas análises de segurança, a taxa de eventos adversos de grau igual ou superior a 3 foi de 25% no tratamento com T-DM1, destacando-se como principais eventos a ocorrência de fadiga, náuseas, elevação de transaminases hepáticas, mialgia, artralgia e plaquetopenia.
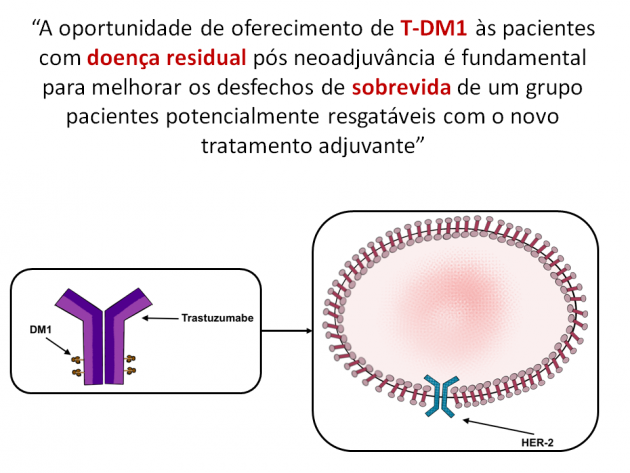
Dra. Debora Gagliato destaca: “trata-se de importante opção terapêutica para pacientes com doença HER-2 positiva que falham em atingir resposta patológica completa com nosso melhor tratamento disponível, poliquimioterapia em combinação à trastuzumabe e pertuzumabe. Sabemos que esse grupo de pacientes possui um risco altíssimo de recidiva, proporcional ao volume de doença residual, sendo recaída de doença sistêmica a modalidade mais comum de recorrência nesse grupo. O estudo mostrou de forma bastante clara que a substituição de trastuzumabe por T-DM1 na adjuvância dessas pacientes foi principalmente capaz de reduzir o risco de recidivas à distância, a qual é potencial causa de morbi-mortalidade nessa população. Com a aprovação, é fundamental interação de cirurgiões e oncologistas para encaminhamento para tratamento neoadjuvante das pacientes diagnosticadas com doença HER-2 positiva. A oportunidade de oferecimento de T-DM1 às pacientes com doença residual pós neoadjuvância é fundamental para melhorar os desfechos de sobrevida de um grupo pacientes potencialmente resgatáveis com o novo tratamento adjuvante”.
Por Dr. Daniel Vargas P. de Almeida
