Continue sua leitura
Nivolumabe recebe nova aprovação no cenário do câncer de pulmão ressecável nos EUA
Em 3 de outubro de 2024, o FDA (Food and Drug Administration) aprovou o uso de nivolumabe em combinação com quimioterapia baseada em platina como tratamento neoadjuvante para câncer de pulmão de células não pequenas (CPCNP) ressecável (tumores ≥ 4 cm e/ou linfonodo positivo). O regime inclui o uso de nivolumabe como agente único no tratamento adjuvante após cirurgia. A aprovação é destinada a pacientes adultos cujos tumores não apresentem mutações conhecidas no gene EGFR ou rearranjos do gene ALK.
O uso de nivolumabe no tratamento perioperatório foi avaliado no estudo de fase III CheckMate 77T, que randomizou 461 pacientes com CPCNP ressecável (estádios IIA a IIIB) entre receber nivolumabe ou placebo em combinação com quimioterapia à base de platina por até 4 ciclos, seguidos por nivolumabe monoterapia ou placebo por até 13 ciclos pós-operatórios. Dentre as características dos pacientes incluídos, a idade mediana foi de 66 anos. Sobre as características dos tumores, 56% tinham tumores com expressão de PD-L1 ≥ 1%, 35% tinham doença em estádio II, 64% tinham doença em estádio III, 23% tinham doença N1, 39% tinham doença N2, 51% tinham tumores com histologia escamosa e 49% tinham tumores com histologia não escamosa. Sobre o histórico dos pacientes, 90% eram tabagistas ou ex-tabagistas. Cirurgia definitiva foi executava em 78% dos pacientes no braço nivolumabe e 77% daqueles no braço de placebo.
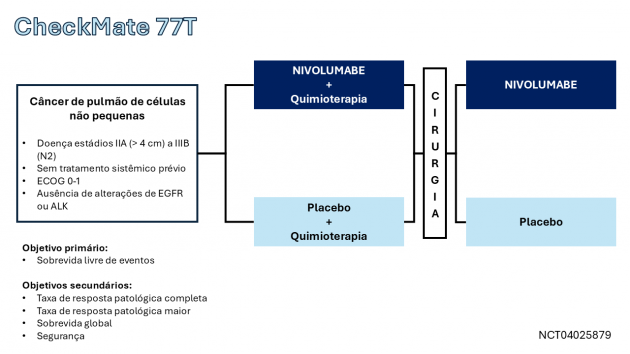
O desfecho primário foi a sobrevida livre de eventos, que apresentou uma mediana não alcançada no grupo nivolumabe, comparada a 18,4 meses no grupo placebo, com uma redução de risco de 42% (HR=0,58; IC de 95%: 0,43-0,78; p=0,00025). Os dados de sobrevida global ainda são imaturos. Os eventos adversos observados foram consistentes com outros estudos de nivolumabe em combinação com quimioterapia. No tratamento neoadjuvante, 5,3% dos pacientes no grupo nivolumabe não puderam realizar a cirurgia devido a eventos adversos, comparados a 3,5% no grupo placebo. Além disso, 4,5% dos pacientes no grupo nivolumabe tiveram atraso na cirurgia devido a reações adversas, versus 3,9% no grupo placebo.
Por Dr. Daniel Vargas P. de Almeida
