Continue sua leitura
Carcinoma hepatocelular recebe aprovação de nova opção de tratamento nos EUA
O carcinoma hepatocelular, principal neoplasia primária do fígado, acomete cerca de 42 mil novos pacientes anualmente nos Estados Unidos, sendo responsável por aproximadamente 31 mil mortes ao ano. Desde 10 de maio os pacientes portadores dessa neoplasia agora possuem uma nova opção de tratamento aprovada pelo FDA (Food and Drug Administration), trata-se do anticorpo monoclonal ramucirumabe, baseado nos dados do estudo REACH-2.
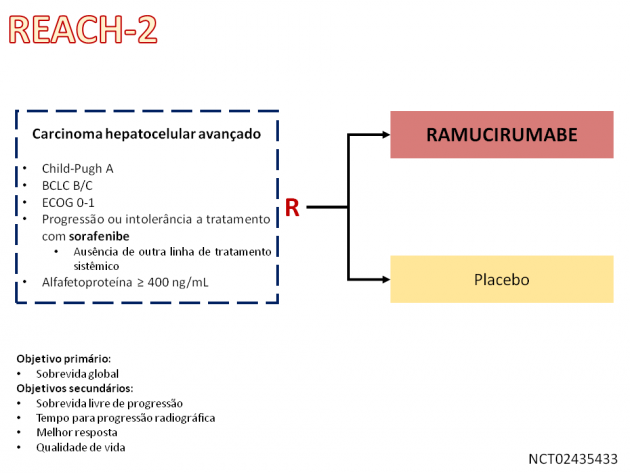 Neste estudo de fase III, 292 pacientes portadores carcinoma hepatocelular avançado com progressão a tratamento de primeira linha com sorafenibe e nível sérico de alfafetoproteína ≥ 400 ng/mL foram randomizados para receber ramucirumabe ou placebo até progressão de doença, morte ou toxicidade limitante. Aproximadamente metade dos pacientes incluídos no estudo eram de origem asiática. Foram contemplados aqueles com etiologia por infecção viral pelo vírus B, bem como pelo vírus C, importantes fatores etiológicos do carcinoma hepatocelular. Após um seguimento mediano de 7,6 meses, o estudo atingiu seu objetivo primário, promovendo uma redução de 29% no risco relativo de morte com o uso de ramucirumabe (HR=0,71; IC de 95%: 0,53-0,95; p=0,02).
Neste estudo de fase III, 292 pacientes portadores carcinoma hepatocelular avançado com progressão a tratamento de primeira linha com sorafenibe e nível sérico de alfafetoproteína ≥ 400 ng/mL foram randomizados para receber ramucirumabe ou placebo até progressão de doença, morte ou toxicidade limitante. Aproximadamente metade dos pacientes incluídos no estudo eram de origem asiática. Foram contemplados aqueles com etiologia por infecção viral pelo vírus B, bem como pelo vírus C, importantes fatores etiológicos do carcinoma hepatocelular. Após um seguimento mediano de 7,6 meses, o estudo atingiu seu objetivo primário, promovendo uma redução de 29% no risco relativo de morte com o uso de ramucirumabe (HR=0,71; IC de 95%: 0,53-0,95; p=0,02).
No tocante à toxicidade, a taxa de eventos adversos sérios associados ao tratamento com ramucirumabe foi de 35%, e as toxicidades mais comuns apresentadas pelos pacientes foram fadiga, edema periférico, hipertensão e hiporexia.
“Essa é mais uma opção de tratamento para pacientes que falharam a inibidores de VEGF em primeira linha, a qual sugere que a continuidade da inibição desta via constitui uma importante ferramenta para o manejo destes pacientes”, comenta Dr. Lucas V. dos Santos, oncologista da BP – A Beneficência Portuguesa de São Paulo.
Por Dr. Daniel Vargas P. de Almeida
