Continue sua leitura
Atezolizumabe recebe nova aprovação para o tratamento do câncer de pulmão avançado no Brasil
O câncer de pulmão é uma neoplasia com grande incidência na população brasileira, bem como em todo o mundo. As estatísticas nacionais demonstram que para o ano de 2018, estima-se a ocorrência de aproximadamente 31.000 novos casos da doença, com cerca de 26.000 mortes em consequência da mesma. A taxa de sobrevida em 5 anos no cenário nacional ainda é bastante baixa (18%), principalmente em decorrência da alta taxa de casos diagnosticados no cenário avançado (84%).
Aumentando as opções de tratamento para essa neoplasia no cenário nacional, a ANVISA (Agência Nacional de Vigilância Sanitária) divulgou em 09 de julho de 2019 a aprovação do regime quimioterápico combinado de carboplatina e paclitaxel associado aos anticorpos monoclonais atezolizumabe e bevacizumabe para o tratamento de primeira linha dos pacientes com câncer de pulmão de células não pequenas e histologia não escamosa de acordo com os dados do estudo de fase III IMpower-150. Diferentemente da aprovação em bula americana pelo FDA (Food and Drug Administration), os pacientes com mutação sensibilizadora nos genes EGFR e ALK estão contemplados na aprovação pela ANVISA, conquanto que haja exposição prévia a terapia-alvo.
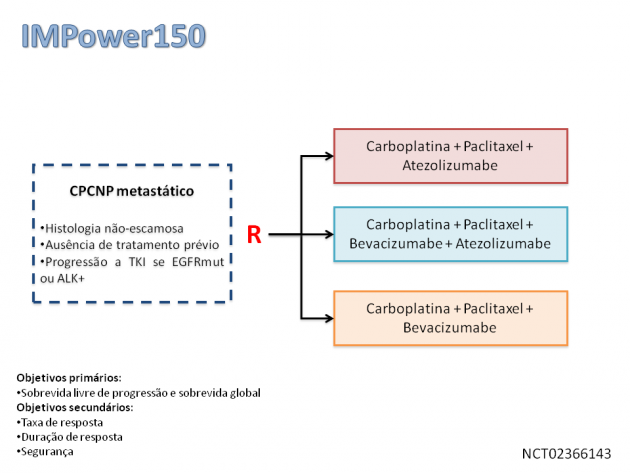
Nesse estudo, 1.202 pacientes com câncer de pulmão de células não pequenas metastático de histologia não escamosa foram randomizados para receber um dentre três diferentes regimes de tratamento de primeira linha: carboplatina + paclitaxel + atezolizumabe + bevacizumabe (braço 1), carboplatina + paclitaxel + atezolizumabe (braço 2), ou carboplatina + paclitaxel + bevacizumabe (braço 3). A inclusão de pacientes com alterações sensibilizadoras a terapia-alvo no ALK ou EGFR era permitida apenas caso apresentassem progressão ao tratamento prévio com inibidor de tirosina quinase. O tratamento quimioterápico foi administrado por 4 a 6 ciclos, sendo então modificado para a manutenção com atezolizumabe e/ou bevacizumabe de acordo com os regimes de tratamento inicialmente propostos. Com um seguimento mediano de cerca de 15 meses, os pacientes com ausência de mutações driver tratados com o regime de 4 drogas (braço 1) apresentaram benefício estatisticamente significativo em sobrevida livre de progressão (HR=0,62; IC de 95%: 0,52-0,74; p<0,001), bem como em sobrevida global (HR=0,78; IC de 95%: 0,64-0,96; p=0,02) quando comparados aos que receberam regime padrão de 3 drogas (braço 3). A taxa de resposta atingida também foi numericamente superior para o braço 1 quando comparado ao braço 3 (55% versus 42%). No tocante a segurança, a taxa de eventos adversos sérios foi de 25,4% no braço 1 e 19,3% no braço 3. Os eventos adversos mais comuns foram fadiga, alopecia, náusea, diarreia, constipação, inapetência, artralgia, hipertensão e neuropatia. As demais toxicidades foram semelhantes aos dados prévios da utilização dessas drogas em outros cenários.
“A aprovação coloca à disposição de oncologistas e pacientes mais um regime de quimioimunoterapia para pacientes com câncer de pulmão de células não pequenas e histologia não escamosa. Há especial interesse no uso desta estratégia para pacientes com mutações de EGFR que falharam TKI e necessitam de tratamento quimioterápico. Esse subgrupo foi representado no estudo IMpower-150 e beneficiou-se da combinação, ilustrando um potencial benefício da associação de quimioterapia, antiangiogênicos e imunoterapia especificamente neste contexto”, destaca o Dr. William William, oncologista e diretor médico da Oncologia Clínica e Hematologia do Centro Oncológico da BP – A Beneficência Portuguesa de São Paulo.
Por Dr. Daniel Vargas P. de Almeida
