Continue sua leitura
Aprovado novo tratamento para leucemia de células pilosas no Brasil
A ANVISA (Agência Nacional de Vigilância Sanitária) aprovou em 03 de agosto de 2020 a imunotoxina moxetumomabe pasudotox para o tratamento de pacientes adultos com leucemia de células pilosas recidivada ou refratária previamente tratados com pelo menos duas terapias sistêmicas, incluindo um análogo do nucleosídeo purina. A droga consiste na fusão de um anticorpo anti-CD22, proteína transmembrana altamente expressa nas células tumorais, com a toxina PE38.
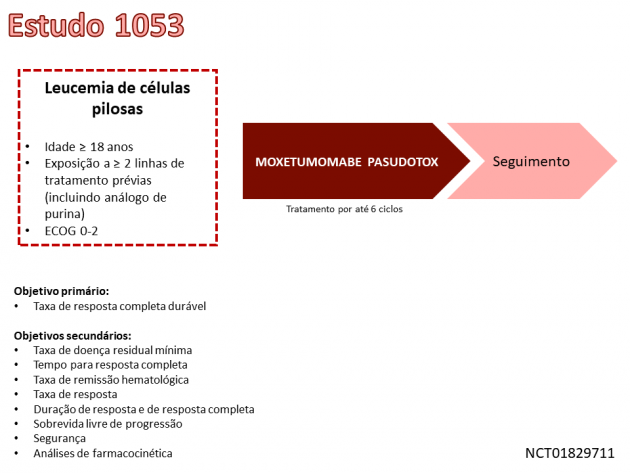
A aprovação é baseada em um estudo multicêntrico de braço único fase III com 80 pacientes. A taxa de resposta completa durável (duração > 180 dias), objetivo primário do estudo, foi 36,3% na avaliação pelo comitê independente, com 32% dos pacientes mantendo resposta completa por ao menos 360 dias. Dentre os demais desfechos de eficácia, a taxa de resposta objetiva foi 75%, com duração mediana de resposta de 66,7 meses, duração mediana de resposta completa de 62,8 meses e sobrevida livre de progressão mediana de 41,5 meses. Na análise de segurança, a taxa de eventos adversos sérios foi 35%, destacando-se edema, hipoalbuminemia, elevação de transaminases, náusea e reações infusionais como os eventos mais comuns.
A dose de tratamento recomendada é moxetumomabe pasudotox, 0,04 mg/kg, IV nos dias 1, 3 e 5 a cada 28 dias. A aprovação teve análise priorizada por tratar-se de medicamento destinado para o tratamento de doença rara.
Por Dr. Daniel Vargas P. de Almeida
