Continue sua leitura
ANVISA aprova nova opção de tratamento com combinação de imunoterapias para o câncer de pulmão avançado
A ANVISA (Agência Nacional de Vigilância Sanitária) aprovou em 13 de novembro de 2023 o regime combinado de durvalumabe com tremelimumabe associados a quimioterapia baseada em platina para o tratamento de primeira linha de pacientes com câncer de pulmão de células não pequenas (CPCNP) metastático sem alterações de EGFR ou ALK.
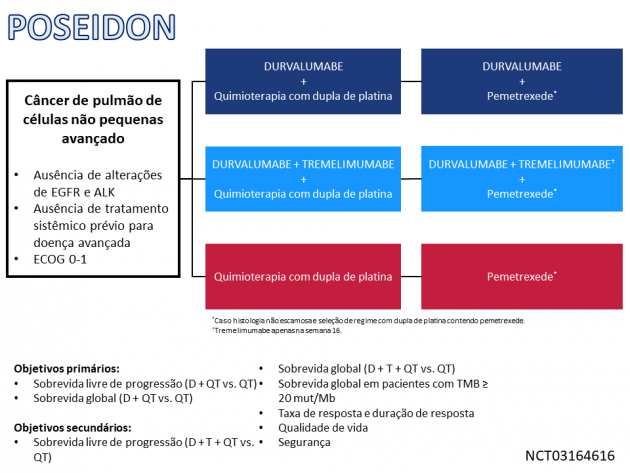
O tratamento utilizando a combinação dos inibidores de PD-L1 e CTLA-4 foi estudado no estudo de fase III POSEIDON que randomizou pacientes com CPCNP avançado sem tratamento sistêmico prévio a uma razão 1:1:1 entre: tremelimumabe + durvalumabe + quimioterapia com dupla de platina por 4 ciclos seguidos de manutenção com durvalumabe e 1 ciclo adicional de tremelimumabe (braço 1), durvalumabe e quimioterapia com dupla de platina por 4 ciclos seguidos de manutenção com durvalumabe (braço 2), ou quimioterapia com dupla de platina por até 6 ciclos (braço 3). Os regimes quimioterápicos permitidos foram carboplatina + nab-paclitaxel, cis/carboplatina + gencitabina e cis/carboplatina + pemetrexede, sendo que neste último foi permitida a estratégia de manutenção com pemetrexede a critério do investigador. A aprovação foi baseada na análise comparativa de 675 pacientes randomizados entre os braços 1 e 3. A idade mediana dessa população foi 63 anos (46% possuíam ≥ 65 anos), 79% possuíam histórico de tabagismo ativo ou prévio, 63% apresentavam histologia não escamosa e 29% possuíam expressão de PD-L1 ≥ 50% nas células tumorais.
O regime com os imunoterápicos demonstrou benefícios em sobrevida livre de progressão (6,2 versus 4,8 meses – HR=0,72; IC de 95%: 0,60-0,86; p=0,0003), sobrevida global (14,0 versus 11,7 meses – HR=0,77; IC de 95%: 0,65-0,92; p=0,0030), taxa de resposta confirmada (38,8% versus 24,4%) e duração de resposta (9,5 versus 5,1 meses). A taxa de eventos adversos sérios no braço de durvalumabe e tremelimumabe foi 44%, incluindo 4,2% de eventos fatais, e a taxa de descontinuação do tratamento devido eventos adversos foi 17%. Os eventos adversos mais frequentes em qualquer grau foram: náuseas, fadiga, dor musculoesquelética, redução do apetite, rash cutâneo e diarreia.
Por Dr. Daniel Vargas P. de Almeida
