Continue sua leitura
Olaparibe é aprovado nos EUA como nova opção de tratamento de manutenção do câncer de ovário avançado
O uso do inibidor de PARP (poli ADP-ribose polimerase) olaparibe foi aprovado pela agência regulatória norte-americana Food and Drug Administration (FDA) para tratamento de manutenção após quimioterapia nas pacientes com carcinoma epitelial de ovário avançado portadoras de mutação do gene BRCA no dia 19 de dezembro de 2018.
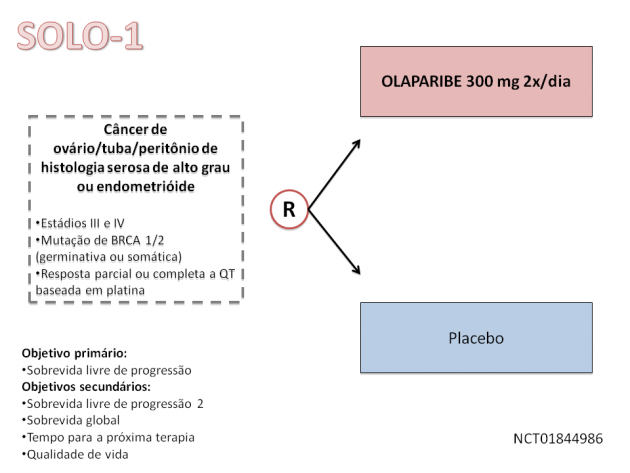
A terapia de manutenção com olaparibe no câncer de ovário avançado é baseada no estudo de fase III SOLO-1, que randomizou 391 pacientes com tumores de ovário, peritônio ou tuba uterina de histologia serosa de alto grau ou endometrióide, portadoras de mutação germinativa ou somática do BRCA1 ou BRCA2 nos estádios III a IV com resposta parcial ou completa a tratamento quimioterápico baseado em platina para receberem terapia de manutenção com olaparibe ou placebo (2:1). Após um seguimento mediano de 41 meses, a terapia de manutenção com olaparibe promoveu uma redução relativa de 70% no risco de progressão de doença ou morte quando comparado a placebo (HR=0,3; IC de 95%: 0,23-0,41; p<0,001). Em relação à sobrevida global, a análise interina dos dados aponta para uma tendência de benefício com o uso de olaparibe, apesar do baixo número de eventos (HR=0,95; IC de 95%: 0,6-1,53). A taxa de eventos adversos com o uso de olaparibe foi consistente com os estudos prévios utilizando essa droga, demonstrando uma taxa de eventos de graus 3-4 de 39% versus 18% para placebo, a despeito do período mais prolongado de uso da droga.
Associado ao tratamento, também foi aprovado o teste diagnóstico para detecção da mutação de BRCA chamado BRCAnalysis CDx test, que utiliza as metodologias por reação de cadeia de polimerase (PCR) e sequenciamento de Sanger. 
“Esse importante estudo reforça o papel dos inibidores da PARP para pacientes BRCA mutadas com câncer de ovário, demonstrando grande redução de risco de progressão de doença ou morte com seu uso também em pacientes recém-diagnosticadas com essa doença”, ressalta a Dra. Juliana Martins Pimenta, oncologista da BP – A Beneficência Portuguesa de São Paulo. “É importante lembrar que cerca de 15% das pacientes com câncer de ovário têm mutação de BRCA, e que todas as pacientes com esse diagnóstico têm indicação de realizar avaliação oncogenética, com importância ainda maior diante dos dados cada vez mais robustos do uso de inibidores da PARP para o tratamento dessa doença. O olaparibe já é aprovado no Brasil para uso em pacientes com câncer de ovário recorrente platino sensível com mutação de BRCA (germinativa e somática)” complementa.
Por Dr. Daniel Vargas P. de Almeida
Veja também:
- Cobertura da ESMO 2018 em vídeo – Dras. Angélica Nogueira e Aknar Calabrich comentam o estudos SOLO-1
- Notícia “O que muda no MOC após a ESMO 2018”, com comentários sobre o estudo SOLO-1
