Continue sua leitura
Tivozanibe é aprovado para o tratamento do carcinoma de células renais avançado nos EUA
O FDA (Food and Drug Administration) aprovou em 10 de março de 2021 o inibidor de quinase tivozanibe para o tratamento de pacientes com carcinoma de células renais recidivado ou refratário previamente expostos a pelo menos duas linhas de terapia sistêmica.
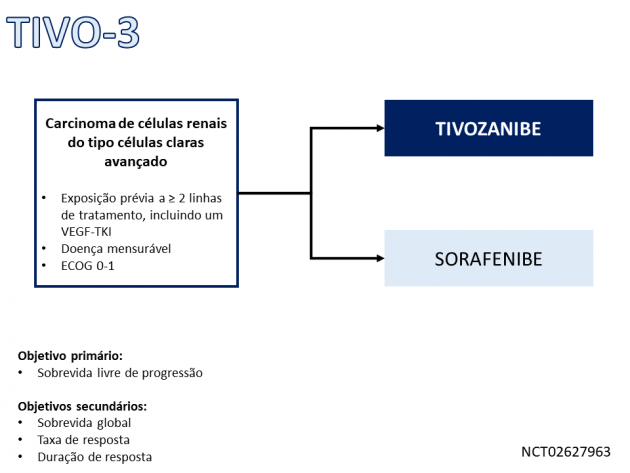
A eficácia do inibidor de quinase foi avaliada no estudo TIVO-3, que comparou o tratamento com tivozanibe e sorafenibe em 350 pacientes com carcinoma de células renais. A sobrevida livre de progressão, objetivo primário do estudo, foi de 5,6 versus 3,9 meses nos braços tivozanibe e sorafenibe, respectivamente (HR=0,73; IC de 95%: 0,56-0,95; p=0,016). A sobrevida global mediana foi de 16,4 meses para tivozanibe e 19,2 meses para sorafenibe (HR=0,97; IC de 0,75-1,24). A taxa de resposta objetiva foi de 18% e 8% para tivozanibe e sorafenibe, respectivamente. Na avaliação de segurança, os eventos adversos mais frequentes com tivozanibe foram fadiga, hipertensão arterial, diarreia, redução do apetite, náuseas, disfonia, hipotireoidismo, tosse e estomatite.
A dose de tratamento recomendada é tivozanibe, 1,34 mg via oral, uma vez ao dia por 21 dias a cada 4 semanas.
“Essa aprovação destaca a importância da via da angiogênese no tratamento do carcinoma de células renais, mesmo em pacientes previamente politratados. Merece destaque a maior taxa de resposta proporcionada pelo tratamento com tivozanibe neste cenário, possibilitando oferecer aos pacientes um tratamento com maior eficácia mesmo na doença refratária”, comenta o Dr. Daniel Vargas, oncologista do Grupo Oncoclínicas de Brasília.
Por Dr. Daniel Vargas P. de Almeida
