Continue sua leitura
Novo regime combinado é aprovado para o tratamento de primeira linha do carcinoma de células renais nos EUA
O FDA (Food and Drug Administration) anunciou em 22 de janeiro de 2021 a aprovação do regime combinado do anti-PD-1 nivolumabe com o inibidor de tirosina quinase cabozantinibe para o tratamento de primeira linha do carcinoma de células renais avançado, baseado nos dados do estudo de fase III CheckMate 9ER.
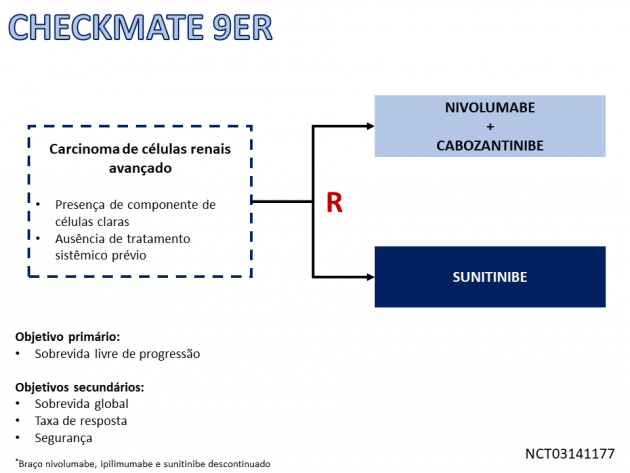
Nesse estudo, 651 pacientes portadores de carcinoma de células renais com um componente de células claras sem terapia sistêmica prévia foram randomizados entre tratamento de primeira linha com sunitinibe ou a combinação de nivolumabe e cabozantinibe. Destaca-se dentre a população incluída no estudo que a maioria dos pacientes (57,6%) possuía risco intermediário pelos critérios IMDC e cerca de um quarto dos pacientes possuía expressão de PDL-1 ≥ 1%. Após um seguimento mediano de 18,1 meses, o regime de tratamento combinado foi associado a uma redução de 49% no risco de progressão de doença ou morte em comparação ao braço sunitinibe (HR=0,51; IC de 95%: 0,41-0,64; p<0,0001), objetivo principal do estudo. Adicionalmente, também houve redução de 40% no risco de morte em favor do braço combinado, com as sobrevidas medianas não atingidas em ambos os grupos (HR=0,60; IC de 98,89%: 0,40-0,89; p=0,0010). A taxa de resposta e a taxa de resposta completa foram aproximadamente o dobro no braço nivolumabe e cabozantinibe em comparação a sunitinibe (55,7% versus 27,1% e 8% versus 4,6%, respectivamente). No tocante a segurança, a taxa de eventos adversos de graus ≥ 3 foi maior no braço do regime combinado (60,6% versus 50,9%), destacando-se diarreia, síndrome mão-pé, hipotireoidismo, hipertensão arterial e fadiga como os eventos adversos de qualquer grau apresentados em maior frequência. As avaliações de qualidade de vida também demonstraram escores melhores nos pacientes do braço nivolumabe e cabozantinibe.
Por Dr. Daniel Vargas P. de Almeida
