Continue sua leitura
Olaparibe combinado a abiraterona é aprovado nos EUA para o tratamento de pacientes com câncer de próstata avançado com alterações de BRCA
No dia 31 de maio de 2023, o FDA (Food and Drug Administration) aprovou o uso de olaparibe combinado a abiraterona para o tratamento de pacientes adultos com câncer de próstata metastático resistente à castração (CPRCm) com mutação deletéria ou possivelmente deletéria nos genes BRCA.
A combinação foi avaliada no estudo de fase III PROpel, que randomizou 796 pacientes para receberem olaparibe com abiraterona ou placebo com abiraterona no tratamento de primeira linha do CPRCm. A avaliação do status mutacional de BRCA foi realizada pelos testes FoundationOne® e FoundationOne Liquid® de maneira retrospectiva. Nas características da população incluída, cerca de 20% haviam recebido docetaxel no cenário castração-sensível, apenas 1 paciente havia recebido tratamento com um novo agente anti-hormonal e cerca de 70% dos pacientes não apresentavam mutação nos genes relacionados ao reparo por recombinação homóloga (HRR).
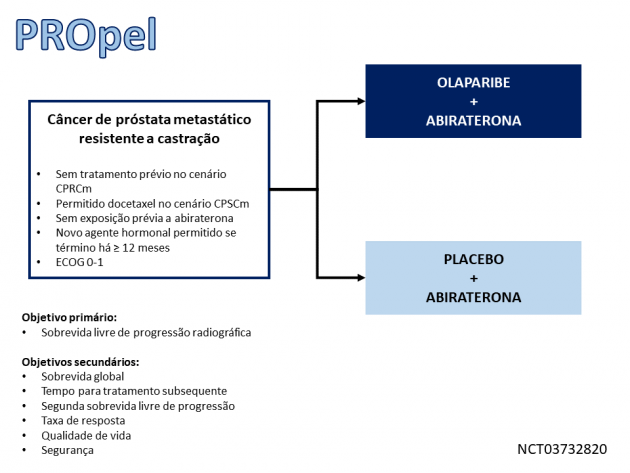
O principal desfecho de eficácia avaliado foi a sobrevida livre de progressão radiológica (SLPr), sendo sobrevida global um dos objetivos secundários. Como resultado, foi demonstrado um benefício estatisticamente significativo na sobrevida livre de progressão radiográfica em favor da combinação de olaparibe com abiraterona quando comparado ao braço placebo com abiraterona na população de intenção de tratamento (HR=0,66; IC de 95%: 0,54-0,81; p<0,001). Uma análise exploratória de subgrupos com 85 pacientes portadores de mutações de BRCA (11% da população) demonstrou uma SLPr mediana não atingida no braço olaparibe com abiraterona, em comparação a 8 meses para aqueles que receberam placebo com abiraterona (HR=0,24; IC de 95%: 0,12-0,45), além também de resultado favorável na avaliação de sobrevida global (HR=0,30; IC de 95%: 0,15-0,59). Nos 711 pacientes sem alterações de BRCA, o hazard ratio (HR) de SLPr foi 0,77 (IC de 95%: 0,63-0,96) e o HR de sobrevida global foi 0,92 (IC de 95%: 0,74-1,14), sugerindo que os benefícios observados na população por intenção de tratamento foram principalmente atribuíveis aos pacientes com mutações de BRCA. Os eventos adversos mais comuns (≥10%) em pacientes que receberam olaparibe e abiraterona foram: anemia (48%), fadiga (38%), náuseas (30%), diarreia (19%), diminuição do apetite (16%), linfopenia (14%), tonturas (14%) e dor abdominal (13%). Setenta e dois pacientes (18%) necessitaram de pelo menos uma transfusão de sangue e 46 (12%) necessitaram de múltiplas transfusões.
Por Dr. Daniel Vargas P. de Almeida
