Continue sua leitura
Darolutamida aprovada no Brasil para o tratamento de pacientes com câncer de próstata não metastático
No dia 23 de dezembro a ANVISA (Agência Nacional de Vigilância Sanitária) aprovou o antiandrogênico oral darolutamida para o tratamento de pacientes com câncer de próstata não metastático resistente a castração (nmCRPC) conforme os resultados do estudo de fase 3 ARAMIS.
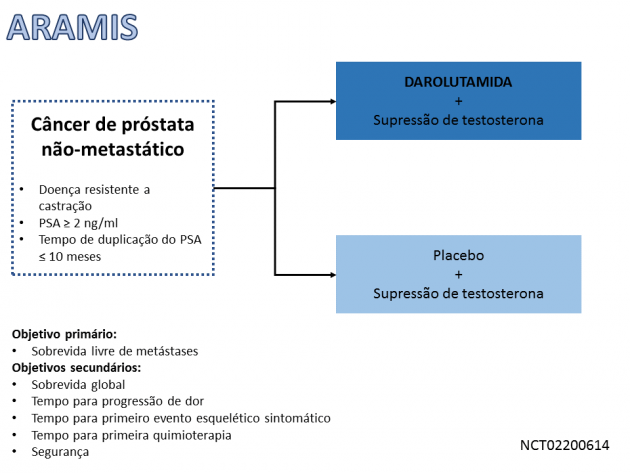
Esse estudo clínico randomizou 1.509 pacientes com doença não metastática resistente a castração de risco alto (PSA ≥ 2 ng/ml e tempo de duplicação do PSA ≤ 10 meses) para receberem darolutamida ou placebo associados a manutenção da terapia de supressão androgênica. O tratamento com darolutamida foi associado a um aumento da sobrevida mediana livre de metástases para 40,4 meses, em comparação a 18,4 meses nos pacientes que receberam placebo, demonstrando um benefício estatisticamente significativo no objetivo primário do estudo (HR para sobrevida livre de metástases= 0,41; IC de 95%:0,34-0,50; p<0,001). Os dados de sobrevida global ainda são imaturos, mas sugerem benefício com o uso da droga (HR=0,71; IC de 95%:0,50-0,99). O tempo para progressão de dor, bem como tempo para início de quimioterapia e para desenvolvimento de evento esquelético sintomático também foram maiores nos pacientes tratados com darolutamida.
No tocante a segurança do tratamento, o uso de darolutamida foi associado a uma taxa de eventos adversos de graus igual ou superior a 3 em 24,7% dos pacientes, sendo os mais comuns: fadiga, dor em extremidades e rash cutâneo.
“A darolutamida é o terceiro inibidor do receptor de androgênio de última geração a ser aprovado no Brasil pela ANVISA no cenário nmCRPC, juntamente com a enzalutamida e a apalutamida. O que chama atenção no estudo da darolutamida é o perfil de toxicidade bastante favorável, sem grandes diferenças nas incidências de eventos adversos quando comparado com placebo. Adicionalmente, quando comparado indiretamente com o perfil de toxicidade de enzalutamida e apalutamida neste cenário parece também ter um perfil discretamente mais favorável, ressaltando-se a cautela na realização de comparações indiretas entre diferentes estudos, devido a particularidades nas características da população recrutada. O racional que poderia estar associado a esse resultado seria o fato de a darolutamida ter uma estrutura molecular bastante distinta de enzalutamida e apalutamida e não cruzar a barreira hemato-encefálica. Quem ganha são os pacientes que passam a contar com mais uma opção no cenário nmCRPC”, destaca o Dr. Fabio Schutz, oncologista da BP – A Beneficência Portuguesa de São Paulo.
“Considero importante enfatizar que este cenário é provavelmente bastante reduzido na prática clínica atual com uso de PET-CT PSMA Ga-68, portanto é necessária a continuação de estudos com darolutamida, buscando levar esta nova opção também para outros cenários mais comuns como a doença metastática sensível a castração, bem como a resistente a castração. Neste sentido, temos o estudo randomizado ARASENS em andamento avaliando o benefício da adição de darolutamida no cenário mCSPC conjuntamente com ADT e docetaxel”, complementa.
Por Dr. Daniel Vargas P. de Almeida
