Continue sua leitura
Ivosidenibe recebe aprovação da ANVISA para o tratamento do câncer de vias biliares
Em 16 de abril de 2024, a ANVISA (Agência Nacional de Vigilância Sanitária) aprovou o uso do inibidor de IDH1 ivosidenibe para o tratamento de pacientes portadores de colangiocarcinoma localmente avançado ou metastático previamente expostos a uma linha de tratamento sistêmico e que apresentem mutação R132 do gene IDH1. As alterações do IDH1 estão presentes em até 20% dos colangiocarcinomas intra-hepáticos, tornando esta via atrativa no desenvolvimento de terapias-alvo para esta doença.
Os dados que embasaram esta aprovação derivam do estudo ClarIDHy, no qual 185 pacientes portadores de colangiocarcinoma localmente avançado ou metastático com mutação de IDH1, previamente expostos a 1 ou 2 regimes terapêuticos prévios contendo gencitabina ou fluoropirimidina foram randomizados entre ivosidenibe ou placebo. Destaca-se que o cross over foi permitido após progressão de doença no braço placebo. Dentre a população incluída, 47% apresentavam história prévia de exposição a 2 regimes de tratamento, a maioria dos pacientes tinha o diagnóstico de colangiocarcinoma intra-hepático (91%) e 92% apresentavam doença metastática. As mutações de IDH1 mais frequentes foram R132C (70%), R132L (15%) e R132G (12%).
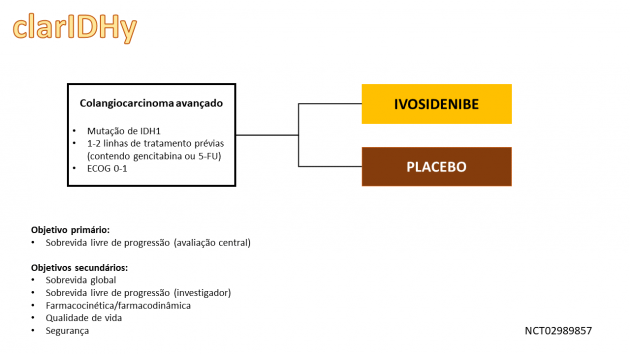
O estudo atingiu seu objetivo primário, com sobrevida livre de progressão de 2,7 versus 1,4 meses em favor do braço experimental (HR=0,37; IC de 95%: 0,25-0,54; p<0,0001). A taxa de resposta a ivosidenibe foi 2,4%, com taxa de controle de doença de 53%, enquanto os mesmos desfechos foram 0 e 28% no braço de placebo. Na avaliação final da sobrevida global, a sobrevida global mediana foi 10,3 versus 7,5 meses para ivosidenibe e placebo, respectivamente (HR=0,79; IC de 95%: 0,56-1,12; p = 0,09). Entretanto na análise ajustada por crossover (o que ocorreu em 70% dos pacientes do braço placebo), o desfecho demonstrou significância estatística em favor de ivosidenibe (HR=0,49; IC de 95%: 0,34-0,70; p < 0,001). Os eventos adversos mais frequentes com a terapia-alvo foram: fadiga, náuseas, dor abdominal, diarreia, tosse e redução do apetite, e eventos adversos graves ocorreram em 34% dos pacientes. Deve-se tomar cuidados especiais na administração concomitante de ivosidenibe com outras drogas que possam cursar com aumento do intervalo QTc.
Por Dr. Daniel Vargas P. de Almeida
