Continue sua leitura
Imunoterapia aprovada pela ANVISA para o tratamento de primeira linha do colangiocarcinoma avançado
A ANVISA (Agência Nacional de Vigilância Sanitária) aprovou em 17 de outubro de 2022 o uso de durvalumabe em associação a gencitabina e cisplatina no tratamento de primeira linha de pacientes com tumores de vias biliares localmente avançados ou metastáticos.
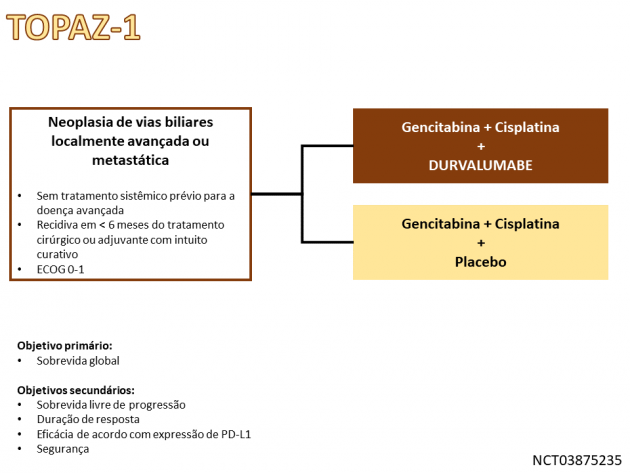
Essa combinação foi avaliada no estudo de fase III TOPAZ-1, que randomizou 685 pacientes com carcinoma de vias biliares localmente avançado ou metastático sem tratamento sistêmico prévio nesse cenário entre durvalumabe ou placebo combinados a gencitabina e cisplatina. Foi permitida a inclusão de pacientes com doença recidivada após cirurgia e tratamento adjuvante desde que o intervalo entre o término da adjuvância e a recorrência de doença fosse superior a 6 meses. Dentre os pacientes incluídos, 50% eram do sexo masculino, 52% eram de origem asiática, 47% possuíam idade ≥ 65 anos, o sítio primário era colangiocarcinoma intra-hepático em 56% deles, colangiocarcinoma extra-hepático em 18% e carcinoma de vesícula biliar em 25%, 20% apresentavam doença recidivada e 86% possuíam doença metastática.
Os resultados atualizados apresentados na ESMO 2022 demonstraram que a combinação de durvalumabe ao regime quimioterápico reduziu em 24% o risco de morte (HR=0,76; IC de 95%: 0,64-0,91), com medianas de 11,35 versus 12,9 meses. A taxa de sobrevida aos 24 meses foi de 23,6% versus 11,5%. A taxa de resposta também foi superior com o regime combinado ao imunoterápico (26,7% versus 18,7%), além de ter sido demonstrada uma correlação entre a resposta ao tratamento e sobrevida global. A taxa de eventos adversos sérios no braço que recebeu tratamento combinado foi de 47%, com 6% de descontinuações em decorrência de eventos adversos. Os eventos adversos sérios que ocorreram em maior frequência foram colangite (7%), febre (3,8%), anemia (3,6%), sepse (3,3%) e insuficiência renal aguda (2,4%). Os eventos adversos mais frequentes em qualquer grau foram: fadiga, náuseas, constipação, redução do apetite, dor abdominal, rash cutâneo e febre.
Por Dr. Daniel Vargas P. de Almeida
Veja também:
