Continue sua leitura
Novo tratamento para câncer hepático aprovado nos Estados Unidos
A agência regulatória norte-americana Food and Drug Administration (FDA) divulgou no dia 16 de agosto de 2018 a aprovação do inibidor de tirosina quinase lenvatinibe para o tratamento de primeira linha do hepatocarcinoma irressecável.
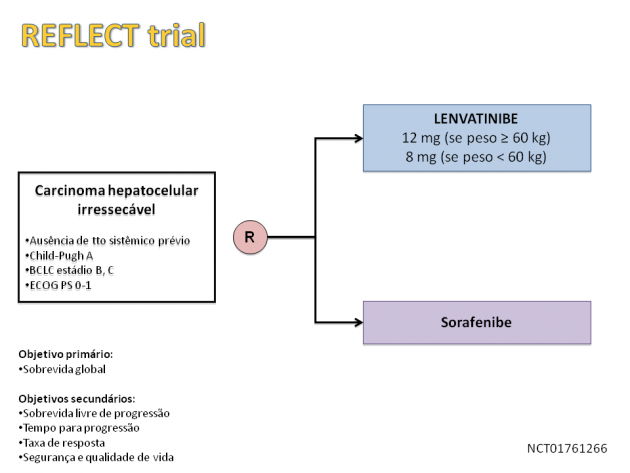
A aprovação do uso de lenvatinibe neste cenário baseia-se no estudo multicêntrico de fase III REFLECT. Neste estudo, 954 pacientes com hepatocarcinoma irressecável sem qualquer tratamento sistêmico prévio foram randomizados para receberem tratamento com lenvatinibe ou outro inibidor de tirosina quinase, sorafenibe. Com um seguimento mediano de cerca de 27 meses, o tratamento com lenvatinibe atingiu o critério de não inferioridade para sobrevida global em comparação ao tratamento com sorafenibe (sobrevida global mediana de 13,6 versus 12,3 meses; HR=0,92; IC de 95%: 0,79-1,06). A sobrevida livre de progressão mediana foi numericamente superior no tratamento com lenvatinibe (7,3 versus 3,6 meses; HR=0,65; p<0,0001) bem como a taxa de resposta (18,8% versus 6,5%).
Em relação à segurança do tratamento, a taxa de efeitos adversos de grau ≥3 foi semelhante entre os braços de tratamento (57% versus 49%), destacando-se que o uso de lenvatinibe foi associado a hipertensão, diarreia, redução do apetite e perda de peso.
A dose recomendada de tratamento é 12 mg uma vez ao dia para pacientes com peso igual ou superior a 60 kg, ou 8 mg no caso de pacientes com peso inferior a 60 kg.
De acordo com o Dr. Ricardo Carvalho, oncologista titular do Departamento de Tumores Gastrointestinais da BP – A Beneficência Portuguesa de São Paulo, “segundo os dados do Global Burden of Disease Cancer Collaboration, o hepatocarcinoma é a quarta causa de morte por câncer no mundo. Até então, sorafenibe era a única droga aprovada na primeira linha de tratamento na doença avançada nos EUA. Recentemente, diversos estudos falharam em demonstrar a não inferioridade ou superioridade de outras drogas em comparação ao sorafenibe. O estudo REFLECT demonstrou que o lenvatinibe é uma excelente alternativa ao sorafenibe na primeira linha, produzindo uma sobrevida global similar, com uma maior SLP e uma maior taxa de resposta, entretanto à custa de toxicidade ligeiramente maior. Desta forma, considero que a aprovação do lenvatinibe na primeira linha é uma excelente notícia para os pacientes nos EUA”. Dr. Ricardo Carvalho ainda acrescenta: “este cenário poderá mudar já nos próximos meses com a apresentação do estudo CheckMate-459, o qual está avaliando a eficácia do nivolumabe na primeira linha”.
Por Dr. Daniel Vargas P. de Almeida
