Continue sua leitura
Pembrolizumabe aprovado para tratamento do CEC de pele avançado nos EUA
O FDA (Food and Drug Administration) aprovou em 24 de junho de 2020 o uso de pembrolizumabe para o tratamento de pacientes com carcinoma de células escamosas (CEC) da pele portadores de doença recorrente ou metastática não considerados passíveis de cura com o emprego de cirurgia ou radioterapia.
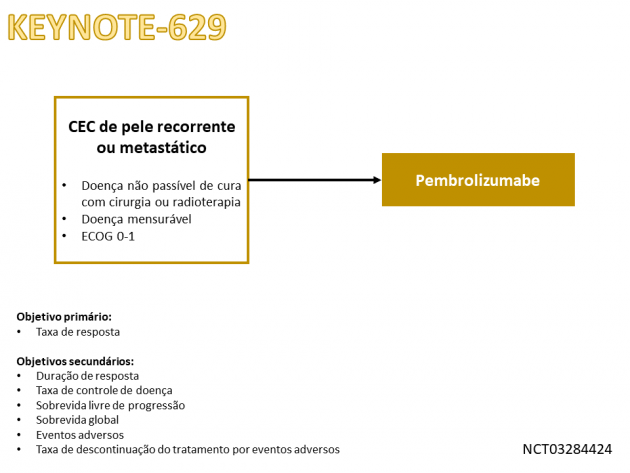
A eficácia do tratamento foi avaliada no estudo KEYNOTE-629, no qual 105 pacientes com CEC de pele avançado foram tratados com pembrolizumabe. O imunoterápico foi administrado na dose de 200 mg a cada 3 semanas e mantido até progressão de doença ou toxicidade limitante por um período máximo de 24 meses. Como resultados, a taxa de resposta objetiva foi 34,3%, com 3,8% de respostas completas, e a taxa de controle de doença (desfecho agregado de doença estável, respostas parciais e completas) foi 52,4%. Após um seguimento mediano de 9,5 meses, a duração mediana de resposta não foi atingida, sendo que 79,5% e 65,6% dos respondedores mantiveram o benefício por período superior a 6 meses e 12 meses, respectivamente. A sobrevida livre de progressão mediana foi 6,9 meses, e a taxa de sobrevida global aos 12 meses foi 60,3%. As análises de segurança demonstraram resultados semelhantes ao uso de pembrolizumabe em outras indicações.
Por Dr. Daniel Vargas P. de Almeida
