Continue sua leitura
Indicação terapêutica de erdafitinibe é atualizada nos EUA
Em 19 de janeiro de 2024, o FDA (Food and Drug Administration) concedeu aprovação definitiva a erdafitinibe para o tratamento de pacientes adultos com carcinoma urotelial localmente avançado ou metastático com alterações de sensibilidade do FGFR3 após exposição prévia a inibidores de PD-1 ou PD-L1. Esta atualização modifica a indicação anteriormente concedida sob aprovação acelerada que incluía todos os pacientes previamente expostos a quimioterapia contendo platina.
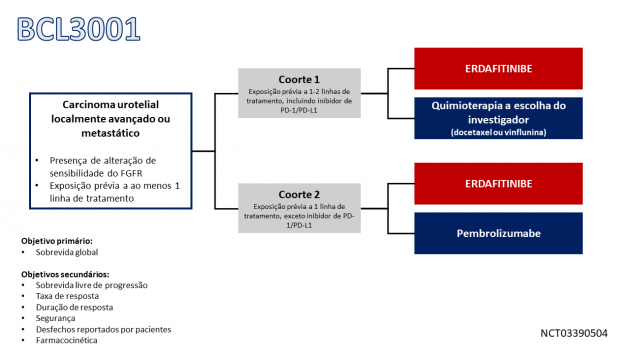
A avaliação de erdafitinibe neste cenário foi conduzida na coorte 1 do estudo BLC3001, que incluiu 266 pacientes com carcinoma urotelial metastático com alterações de sensibilidade do FGFR3 e que haviam recebido 1-2 tratamentos sistêmicos prévios, incluindo um inibidor PD-1 ou PD-L1. Os pacientes foram randomizados entre erdafitinibe ou quimioterapia a escolha do investigador (docetaxel ou vinflunina). A idade mediana dos pacientes era de 67 anos, sendo 71% do sexo masculino, 81% tinham mutações de FGFR3, 17% tinham fusões e 2% tinham ambas mutações e fusões. A localização primária do tumor foi o trato superior para 33% e trato inferior para 67%, 74% dos pacientes tinham metástases viscerais ou ósseas, 88% receberam quimioterapia contendo platina anteriormente e os inibidores PD-1 ou PD-L1 haviam disso administrados no cenário neoadjuvante ou adjuvante em 7% dos pacientes.
A sobrevida global mediana foi de 12,1 meses para pacientes que receberam erdafitinibe e 7,8 meses para aqueles que receberam quimioterapia (HR=0,64; IC de 95%: 0,47-0,88; p=0,0050). A sobrevida livre de progressão mediana foi de 5,6 versus 2,7 meses em favor de erdafitinibe (HR=0,58; IC de 95%: 0,44-0,78; p=0,0002). A taxa de resposta foi de 35,3% com erdafitinibe e 8,5% com quimioterapia (p<0,001). Os eventos adversos mais comuns (> 20%) com o uso de erdafitinibe foram: hiperfosfatemia, alterações ungueais, diarreia, estomatite, elevação de fosfatase alcalina, anemia, elevação de transaminases, hiponatremia, elevação de creatinina, xerostomia, hipofosfatemia, eritrodisestesia palmoplantar, disgeusia, fadiga, xerodermia, constipação, hiporexia, hipercalcemia, alopecia, xeroftalmia, hipercalemia e diminuição de peso.
A modificação da indicação terapêutica decorreu dos resultados da coorte 2 deste mesmo estudo, que randomizou 351 pacientes previamente expostos a uma linha de terapia sistêmica entre erdafitinibe ou pembrolizumabe. O estudo não atingiu seu objetivo primário na avaliação de sobrevida global (HR=1,18; IC de 95%: 0,92-1,51; p=0,18), com medianas de 10,9 meses para erdafitinibe e 11,1 meses para pembrolizumabe.
Por Dr. Daniel Vargas P. de Almeida
