Continue sua leitura
Aprovada no Brasil terapia-alvo para o tratamento do câncer de bexiga avançado
Foi divulgado no Diário Oficial da União em 29 de setembro de 2019 a aprovação de erdafitinibe pela ANVISA (Agência Nacional de Vigilância Sanitária) para o tratamento do carcinoma urotelial avançado após progressão a pelo menos uma linha de tratamento quimioterápico. Trata-se da primeira terapia-alvo aprovada para o tratamento desse tumor no Brasil. Erdafitinibe é um inibidor de tirosina quinase do FGFR (receptor do fator de crescimento de fibroblastos), um gene alterado em aproximadamente 15% a 20% dos tumores uroteliais metastáticos.
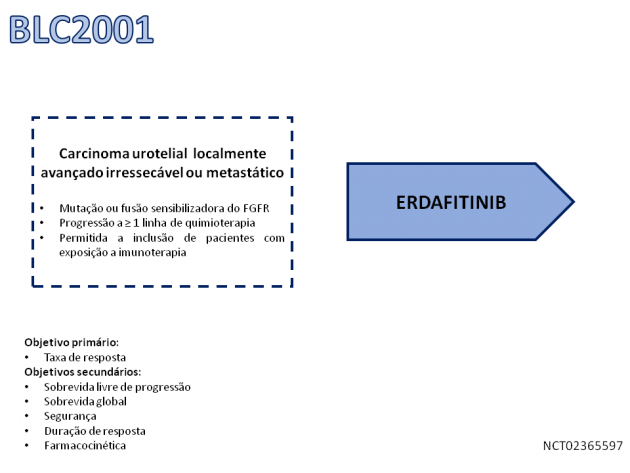
O tratamento com erfabitinibe foi avaliado no estudo de fase II BLC2001, que analisou o tratamento de 99 pacientes com carcinoma urotelial localmente avançado irressecável ou metastático, com progressão a pelo menos uma linha de tratamento quimioterápico (incluindo tratamento adjuvante ou neoadjuvante se realizado há ≤ 12 meses) e portadores de mutações ativadoras do FGFR (mutação do FGFR3, ou fusões no FGFR2 ou FGFR3). A taxa de resposta atingida com o tratamento foi de 40%, incluindo 3% de respostas completas. Dentre a população do estudo, 22% dos pacientes haviam recebido tratamento prévio com inibidores de checkpoint imunológico, e a taxa de resposta nessa população foi de 59%. A sobrevida livre de progressão mediana atingida foi de 5,5 meses, e a sobrevida global mediana de 13,8 meses.
A taxa de eventos adversos relacionados ao tratamento com erdafitinibe de graus igual ou maior a 3 foi de 46%, e taxa de descontinuação do tratamento em decorrência de eventos adversos foi de 13%. Destacam-se entre as toxicidades mais frequentes: alterações na retina (promovendo alterações visuais em até 25% dos pacientes), além de hiperfosfatemia, estomatite, fadiga, elevação de creatinina, alterações do hábito intestinal, xerostomia, onicólise e alterações de enzimas hepáticas.
Por Dr. Daniel Vargas P. de Almeida
