Continúe su lectura
Quimioterapia asociada a atezolizumab y bevacizumab es aprobada para el tratamiento del cáncer de pulmón avanzado en los EUA
El tratamiento del cáncer de pulmón de células no pequeñas avanzadas de histología no escamosa recibió la aprobación de una nueva opción de tratamiento por la agencia estadounidense Food and Drug Administration (FDA) el día 06 de diciembre de 2018. El régimen quimioterápico combinado de carboplatino y el paclitaxel asociado a los anticuerpos monoclonales atezolizumab y bevacizumab fue aprobado para el tratamiento de primera línea de los pacientes con ausencia de alteraciones en el ALK o EGFR, basado en los datos del estudio de fase III IMpower-150.
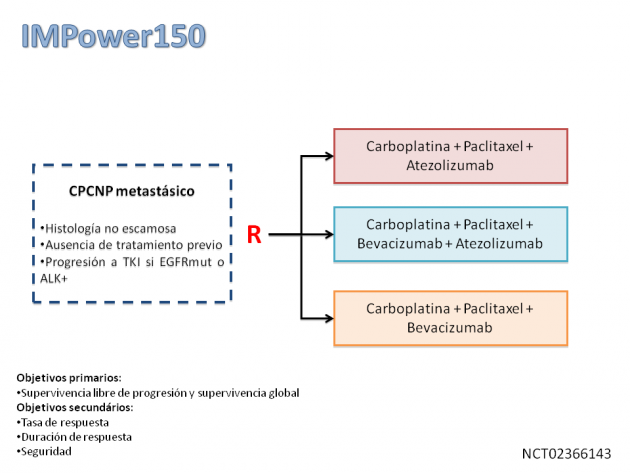
En este estudio, 1202 pacientes con cáncer de pulmón de células no pequeñas metastásicas de histología no escamosa fueron aleatorizados para recibir uno de tres diferentes regímenes de tratamiento de primera línea: carboplatino + paclitaxel + atezolizumab + bevacizumab (brazo 1), carboplatino + paclitaxel + atezolizumab (brazo 2), o carboplatino + paclitaxel + bevacizumab (brazo 3). Se permitió la inclusión de pacientes con alteraciones en el ALK o EGFR si presentaban progresión al tratamiento previo con inhibidor de tirosina quinasa. El tratamiento quimioterápico fue administrado por 4-6 ciclos, siendo entonces modificado para el mantenimiento con atezolizumab y / o bevacizumab de acuerdo con los regímenes de tratamiento inicialmente propuestos. Con un seguimiento mediano de unos 15 meses, los pacientes con ausencia de mutaciones controlador tratados con el régimen de cuatro drogas (brazo 1) presentaron un beneficio estadísticamente significativo en la supervivencia libre de progresión (HR=0,62; IC de 95%: 0,52-0,74; p<0,001), de igual manera en la supervivencia global (HR=0,78; IC de 95%: 0,64-0,96; p=0,02) cuando comparados a los que recibieron régimen padrón de 3 drogas (brazo 3). La tasa de respuesta alcanzada también fue numéricamente superior para el brazo 1 cuando comparado al brazo 3 (55% frente al 42%). En cuanto a la seguridad, la tasa de eventos adversos serios fue de 25,4% en el brazo 1 y el 19,3% en el brazo 3. Los eventos adversos más comunes fueron fatiga, alopecia, náusea, diarrea, constipación, inapetencia, artralgia, hipertensión y neuropatía. Las demás toxicidades fueron similares a los datos previos de la utilización de estos fármacos en otros escenarios.
“Este es otro paso importante en el desarrollo de tratamientos basados en inmunoterapia para el cáncer de pulmón de células no pequeñas (CPCNP). Las tasas de respuesta de la combinación de carboplatino, paclitaxel, bevacizumab y atezolizumab están entre las más altas ya vistas en primera línea para pacientes no mutados, y el aumento en la supervivencia global justifica esta combinación como una opción estándar para los pacientes con CPCNP no escamoso virgen tratamiento metastásico“, como señaló el Dr. William William, Oncólogo y director médico de la Oncología Clínica y Hematología del Centro Oncológico de la BP – La Beneficencia portuguesa de Sao Paulo.
También de acuerdo con el Dr. Carolina Kawamura Haddad, Oncóloga de la BP – La Beneficencia portuguesa de Sao Paulo, “el estudio IMpower-150 incluyó a pacientes con alteraciones de EGFR / ALK, pero una modificación posterior cambió el objetivo primario del estudio para el análisis sólo de los pacientes con ausencia de mutación de controlador. Sin embargo, los resultados en estos pacientes deben ser analizados en un futuro próximo, aunque los datos actuales sugieren beneficio también en esta población“.
Por el Dr. Daniel Vargas P. de Almeida
