Continúe su lectura
Olaparib es aprobado en los EUA como nueva opción de tratamiento de mantenimiento del cáncer de ovario avanzado
El uso del inhibidor de PARP (POLPP-ribosa polimerasa) olaparib fue aprobado por la agencia reguladora norteamericana Food and Drug Administration (FDA) para tratamiento de mantenimiento después de la quimioterapia en las pacientes con carcinoma epitelial de ovario avanzado portadoras de mutación del gen BRCA en el 19 de diciembre de 2018.
La terapia de mantenimiento con olaparib en el cáncer de ovario avanzado se basa en el estudio de fase III SOLO-1, que randomizó a 391 pacientes con tumores de ovario, peritoneo o trompa uterina de histología serosa de alto grado o endometrioide, portadoras de mutación germinativa o somática del BRCA1 o BRCA2 en los estadios III a IV con respuesta parcial o completa al tratamiento quimioterápico basado en platino para recibir terapia de mantenimiento con olaparib o placebo (2: 1). Después de un seguimiento mediano de 41 meses, la terapia de mantenimiento con olaparib ha promovido una reducción relativa del 70% en el riesgo de progresión de enfermedad o muerte en comparación con placebo (HR=0,3; IC de 95%: 0,23-0,41; p<0,001). En cuanto a la supervivencia global, el análisis intermedio de los datos apunta a una tendencia de beneficio con el uso de olaparib, a pesar del bajo número de eventos (HR=0,95; IC de 95%: 0,6-1,53). La tasa de eventos adversos con el uso de olaparib fue consistente con los estudios previos utilizando esta droga, demostrando una tasa de eventos de grados 3-4 de 39% versus a 18% para placebo, a pesar del período más prolongado de uso de la droga.
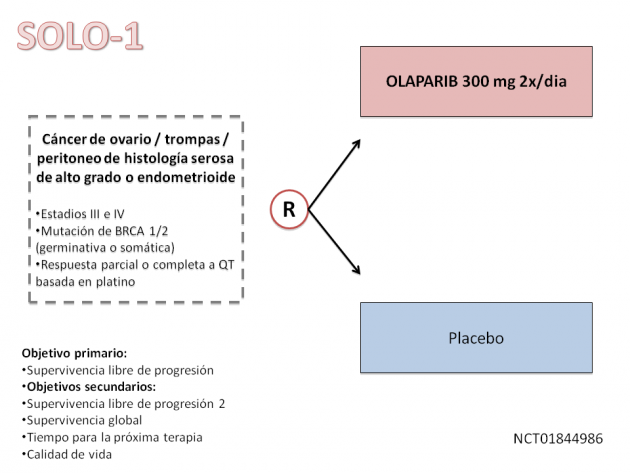
En el presente estudio se analizaron los resultados de la evaluación de la mutación de BRCA llamada BRCAnalysis CDx test, que utiliza las metodologías por reacción de cadena de polimerasa (PCR) y secuenciación de Sanger.
“Este importante estudio refuerza el papel de los inhibidores de la PARP para pacientes BRCA mutados con cáncer de ovario, demostrando gran reducción de riesgo de progresión de enfermedad o muerte con su uso también en pacientes recién diagnosticados con esa enfermedad”, resalta la Dra. Juliana Martins Pimenta, oncóloga de la BP – La Beneficencia Portuguesa de Sao Paulo. “Es importante recordar que cerca del 15% de las pacientes con cáncer de ovario tienen mutación de BRCA, y que todas las pacientes con ese diagnóstico tienen indicación de realizar evaluación oncogenética, con importancia aún mayor ante los datos cada vez más robustos del uso de inhibidores de la PARP para el tratamiento de esta enfermedad. El olaparib ya es aprobado en Brasil para uso en pacientes con cáncer de ovario recurrente platino sensible con mutación de BRCA (germinativa y somática) “complementa.
Por el Dr. Daniel Vargas P. de Almeida
