Continúe su lectura
Cabozantinib está aprobado para el tratamiento de carcinoma hepatocelular avanzado en los EUA
Los pacientes con carcinoma hepatocelular avanzado, el tumor hepático de mayor incidencia y el tercero causante de muerte por cáncer mundial, ahora disponen de una nueva opción de tratamiento aprobada por la agencia estadounidense Food and Drug Administration (FDA). El tratamiento con el inhibidor de tirosina quinasa cabozantinib recibió aprobación el 14 de enero de 2019 para su uso en el tratamiento de los pacientes con enfermedad avanzada que presentaron progresión de enfermedad tras el tratamiento previo con sorafenib.
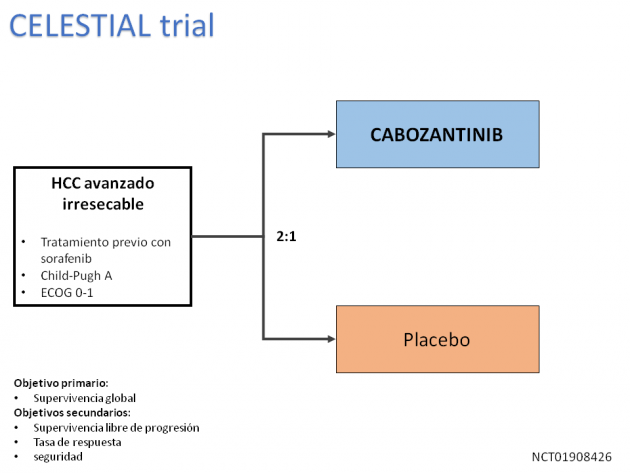
La aprobación se basa en el estudio de fase III CELESTIAL, que evaluó la eficacia y la seguridad del tratamiento en 707 pacientes aleatorizados para recibir cabozantinib o placebo. El tratamiento con el inhibidor de tirosina quinasa se asoció con un aumento de la supervivencia global mediana de 8,0 a 10,2 meses (HR = 0,76; IC del 95%: 0,63-0,92; p = 0,005). La tasa de respuesta al tratamiento con cabozantinib fue del 4%, con una tasa de control de la enfermedad del 64%. Entre los análisis de seguridad, la tasa de eventos adversos de grados 3-4 relacionados con el uso de cabozantinib fue 68% (versus al 36% para el placebo), destacándose entre las toxicidades más frecuentes: síndrome mano-pie, hipertensión arterial, elevación de enzimas hepáticas, fatiga y diarrea.
Como señala el Dr. Fabio Kater, oncólogo de la BP – La Beneficencia Portuguesa de Sao Paulo, “hemos observado un creciente número de estudios que evalúan el tratamiento de segunda línea del carcinoma hepatocelular, mostrando una necesidad médica no alcanzada. La expresión del MET es un conocido mecanismo de resistencia al sorafenib y aumenta conforme el paciente presenta progresión de enfermedad en la primera línea con esa droga. Cabozantinib es una molécula tirosina quinasa inhibidora de esa vía de proliferación, además de ser un antiangiogénico que inhibe la vía del VEGF.
En el estudio CELESTIAL, el cabozantinib en la dosis de 60 mg / día demostró ganancia de supervivencia global en pacientes Child-Pugh A, una población seleccionada, con mejor pronóstico y relativamente difícil de encontrar en la práctica asistencial. Además, la mayoría de la población estaba representada por pacientes occidentales (75%), y portadores de infección por el virus de la hepatitis B (38%). Sin embargo, este estudio también incluyó pacientes de tercera línea y puede ser indicado para esa población no representada en otros trabajos”.
De acuerdo con el mismo, “otro punto favorable con el tratamiento utilizando cabozantinib fue una mayor supervivencia libre de progresión en comparación indirecta con datos de otros estudios (5,2 versus 2-2,5 meses). Sin embargo, la tasa de respuesta fue sólo el 4%, diferente de la que se encuentra con la droga en otras histologías, así como en el uso de otros antiangiogénicos (10-20%) y con uso de inmunoterapia (20%). En cuanto a la toxicidad, las tasas de grados 3-4 se consideraron altas (68%), pero con una tasa de discontinuación relativamente baja (16%)”.
Por el Dr. Daniel Vargas P. de Almeida
