Continúe su lectura
Aprobada combinación de inmunoterapia para el tratamiento del cáncer colorrectal metastásico en los EUA
El 11 de julio del 2018, la agencia reguladora estadounidense Food and Drug Administration (FDA) aprobó la combinación del anticuerpo monoclonal anti-PD-1 nivolumab asociado al anticuerpo monoclonal anti-CTLA-4 ipilumumab para el tratamiento del cáncer colorrectal metastásico en pacientes con inestabilidad de microsatélite-high (MSI-H) o deficiencia de mismatch repair (dMMR), después de una exposición previa al tratamiento sistémico basado en fluoropirimidina, oxaliplatino o irinotecán.
Esta aprobación se basa en los resultados de la tasa de respuesta y la duración de respuesta obtenidos en un subgrupo de pacientes pertenecientes a una de las cohortes del estudio de fase II CheckMate-142. Los pacientes habían recibido al menos una línea de tratamiento previo para la enfermedad metastásica y se sometieron a tratamiento con nivolumab asociado a ipilimumab. De entre la totalidad de 199 pacientes de esa cohorte, 82 de ellos habían recibido algún tratamiento sistémico previo con quimioterapia basada en fluoropirimidina, oxaliplatino e irinotecán.
La tasa de respuesta en la cohorte de 119 pacientes fue del 55%, con el 3,4% de respuestas completas. En el subgrupo de 82 pacientes (subgrupo considerado por la FDA para la aprobación anunciada), la tasa de respuesta alcanzada fue del 46%. La duración media de respuesta del subgrupo aún no se alcanzó, pero el 89% de las respuestas presentadas tuvieron una duración ≥ 6 meses, y el 21% de ellas ≥ 12 meses.
En cuanto a la seguridad, el 86% de los pacientes que concluyó las 4 dosis del tratamiento combinado de nivolumab + ipilimumab, la tasa de eventos adversos graves fue 47%, siendo que los más frecuentes fueron colitis, diarrea, eventos hepáticos, dolor abdominal, insuficiencia renal aguda, fiebre y deshidratación.
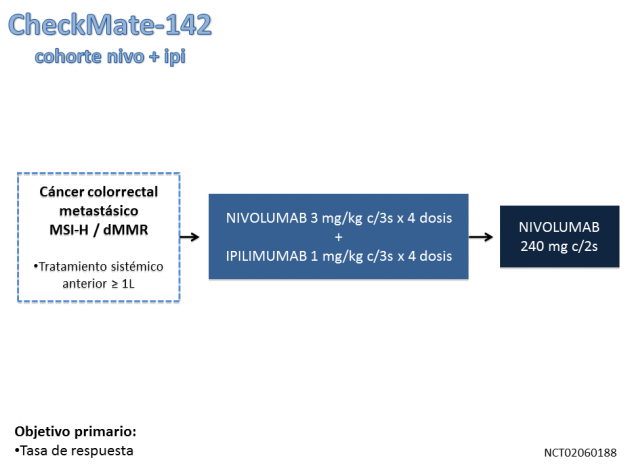
Las dosis recomendadas para tratamiento son: nivolumab 3 mg / kg, asociado a ipilimumab 1 mg / kg, ambos EV cada 3 semanas por 4 dosis, seguidos de mantenimiento con nivolumab 240 mg, EV cada 2 semanas, hasta toxicidad limitante o progresión de enfermedad.
Según el Dr. Fabio Kater, oncólogo BP – La Beneficência Portuguesa de São Paulo, “a partir de los datos actuales de la inmunoterapia en el cáncer de colon, tuvimos la aprobación previa del pembrolizumab cohorte de base de 149 pacientes incluidos en cinco estudios (KEYNOTE -016, -164, -012, -028, e -158) que mostraban una tasa de respuesta en los pacientes iniciales del 40%. Del mismo CheckMate-142, nivolumab aislado proporciona tasa de respuesta del 33%. Es la primera vez que una combinación de inmunoterápicos proporciona una tasa de respuesta del orden del 55% en una población que el 73% de los pacientes ya habían recibido al menos dos líneas previas de tratamiento. Por lo tanto, a la luz de los hallazgos y confrontando con datos paralelos, la combinación de nivolumab y ipilimumab debe ser considerada en pacientes con cáncer de colon metastásico con alta frecuencia de inestabilidad de microsatélite después de, al menos, una línea de tratamiento.”
Por el Dr. Daniel Vargas P. de Almeida
