Continue sua leitura
Combinação de olaparibe e bevacizumabe é aprovada como tratamento de manutenção do câncer de ovário avançado pela ANVISA
A Agência Nacional de Vigilância Sanitária (ANVISA) anunciou em 22 de junho de 2020 a aprovação da combinação do inibidor de PARP olaparibe com o anti-angiogênico bevacizumabe no tratamento de manutenção de pacientes portadoras de câncer epitelial de ovário (tubas uterinas e peritônio) estádios FIGO III-IV que apresentaram resposta (parcial ou completa) à tratamento de primeira linha com quimioterapia baseada em platina associada a bevacizumabe. O regime combinado de manutenção é indicado para pacientes com exposição a ao menos 2 ciclos de bevacizumabe (em casos com cirurgia de debulking de intervalo) ou ao menos 3 ciclos de bevacizumabe em combinação com os últimos 3 ciclos de quimioterapia baseada em platina.
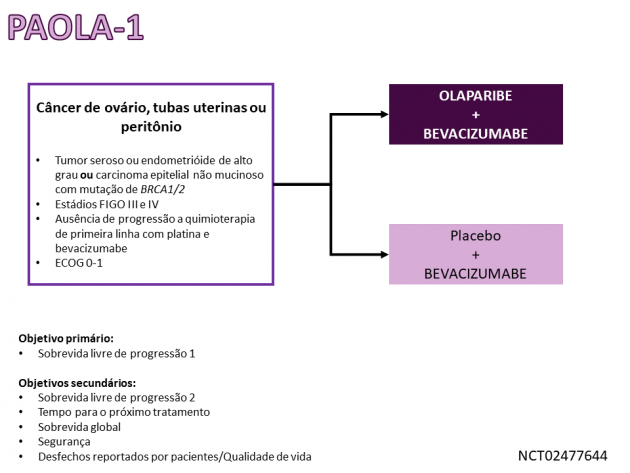
A aprovação do regime de manutenção combinado é baseada nos dados de eficácia do estudo de fase III PAOLA-1 que randomizou 806 pacientes entre bevacizumabe associado a olaparibe (N = 537) ou placebo (N = 269) como tratamento de manutenção após apresentarem resposta a quimioterapia de primeira linha baseada em platina. Com um seguimento mediano de 22,9 meses, a combinação de bevacizumabe e olaparibe foi associada a benefício em sobrevida livre de progressão quando comparado ao uso de bevacizumabe isolado (HR=0,59; IC de 95%: 0,49-0,72; p < 0,001), objetivo primário do estudo, enquanto os dados de sobrevida global ainda são imaturos. Como resultados de segurança, a taxa de eventos adversos de graus ≥ 3 com a combinação de bevacizumabe e olaparibe foi 57%, destacando-se fadiga, náuseas, hipertensão, anemia e linfopenia como os eventos adversos mais comuns de qualquer grau.
O mesmo regime de tratamento foi aprovado recentemente nos Estados Unidos, porém o FDA (Food and Drug Administration) condicionou seu uso à presença de deficiência de recombinação homóloga (definido como a presença de mutação deletéria ou possivelmente deletéria no gene BRCA e/ou instabilidade genômica detectada pelo teste Myriad myChoice®).
Por Dr. Daniel Vargas P. de Almeida
Saiba mais:
