Continue sua leitura
Aprovada imunoterapia para tratamento adjuvante do melanoma no Brasil
Foi aprovado hoje, dia 25 de março de 2019, pela Agência Nacional de Vigilância Sanitária (ANVISA) o tratamento adjuvante com nivolumabe para o melanoma cutâneo com envolvimento de linfonodos ou doença metastática completamente ressecada.
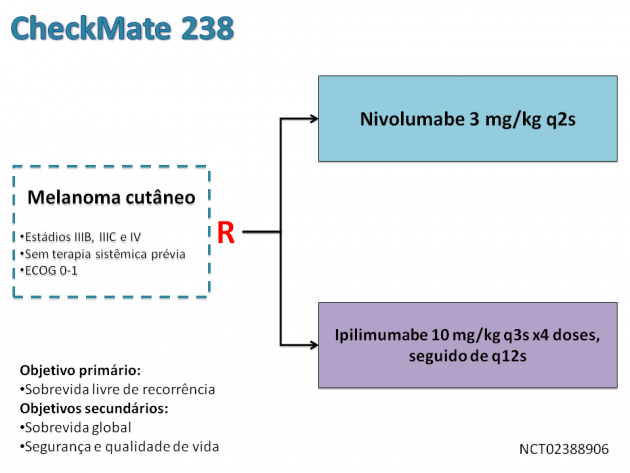
Esta aprovação baseia-se no estudo de fase III CheckMate 238, que randomizou 906 pacientes portadores de melanoma estádios IIIB, IIIC ou IV (AJCC 7ª edição), independente da expressão de PDL-1 e da presença/ausência da mutação de BRAF, com todas as lesões completamente ressecadas cirurgicamente, para receberem nivolumabe ou ipilimumabe adjuvantes pelo período de 1 ano após a cirurgia.
Com um seguimento mediano de 19,5 meses, o estudo atingiu seu objetivo primário, promovendo benefício estatisticamente significativo em sobrevida livre de recorrência em favor do tratamento com nivolumabe (HR=0,65; p<0,001). Tal benefício foi mantido na atualização dos dados, apresentada no último congresso da Sociedade Americana de Oncologia Clínica (ASCO 2018), com um seguimento mínimo de 24 meses, reforçando a redução de 34% no risco de recorrência de doença ou morte (HR=0,66; IC 95%: 0,54-0,81; p<0,0001) promovida pelo uso de nivolumabe em comparação a uma terapia ativa (ipilimumabe). Quando avaliados os diferentes desfechos (recorrência local, regional, à distância, novo tumor primário, morte e toxicidade limitante) o uso de nivolumabe foi associado a melhores resultados em todos os cenários.
No tocante à segurança do tratamento, os dados atualizados demonstram que a taxa de eventos adversos graus ≥ 3 relacionados ao tratamento foi significativamente menor no grupo de pacientes tratados com nivolumabe (14,4% versus 45,9%).
Ressalta-se que esta é a terceira indicação de tratamento do melanoma com nivolumabe aprovada no cenário nacional (previamente o uso de nivolumabe já era aprovado no tratamento do melanoma metastático em monoterapia, bem como em combinação com ipilimumabe).
Por Dr. Daniel Vargas P. de Almeida
Apoio:
Veja também:

