Continue sua leitura
ANVISA aprova TAS-102 para o tratamento do câncer colorretal avançado
A Agência Nacional de Vigilância Sanitária (ANVISA) aprovou em maio de 2020 o quimioterápico oral TAS-102 – um análogo nucleosídeo de administração oral composto de trifluridina (componente ativo) e cloridrato de tipiracila (previne a degradação da trifluridina e tem ação anti-angiogênica) – para o tratamento do câncer colorretal avançado em pacientes previamente tratados com quimioterapia à base de fluoropirimidina, oxaliplatina e irinotecano, terapia anti-VEGF e terapia anti-EGFR (na ausência de mutações do RAS), assim como naqueles pacientes não candidatos a tais terapias. A aprovação de TAS-102 nesse cenário é baseada nos resultados do estudo de fase III RECOURSE.
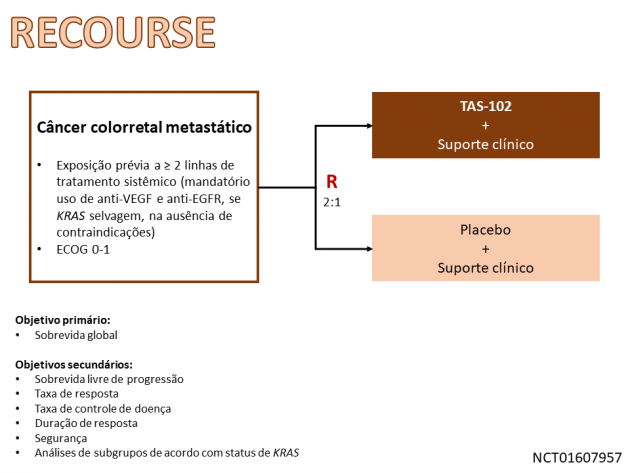
Nesse estudo, 800 pacientes portadores de câncer colorretal previamente expostos a ≥ 2 linhas de tratamento sistêmico foram randomizados a uma proporção de 2:1 entre TAS-102 e placebo. Cerca de metade dos pacientes incluídos no estudo (51% em ambos os braços) apresentavam mutação de KRAS e a maioria deles era extensamente pré-tratada, com 60,9% da população apresentando exposição prévia a ≥ 4 linhas de tratamento sistêmico. O estudo atingiu seu objetivo primário, demonstrando benefício em sobrevida global em favor do braço tratado com TAS-102 (medianas 7,1 versus 5,3 meses; HR=0,68; IC de 95%: 0,58-0,81; p < 0,001), além de demonstrar também benefício em sobrevida livre de progressão (HR=0,48; IC de 95%: 0,41-0,57; p < 0,001). A taxa de resposta objetiva com o uso de TAS-102 foi 1,6% e a taxa de controle de doença avaliada na sexta semana de tratamento foi significativamente superior nesse grupo (44% versus 16%; p < 0,0001). Quanto a segurança do tratamento, a taxa de eventos adversos de graus ≥ 3 foi 69%, no braço que recebeu TAS-102, destacando-se náuseas, vômito, redução do apetite, fadiga e diarreia como os eventos adversos mais comuns em qualquer grau.
A dose recomendada para tratamento é de 35 mg/m² via oral, 2x/dia, do D1 ao D5 e do D8 ao D12, a cada 28 dias, não ultrapassando 80 mg/dose.
Por Dr. Daniel Vargas P. de Almeida
